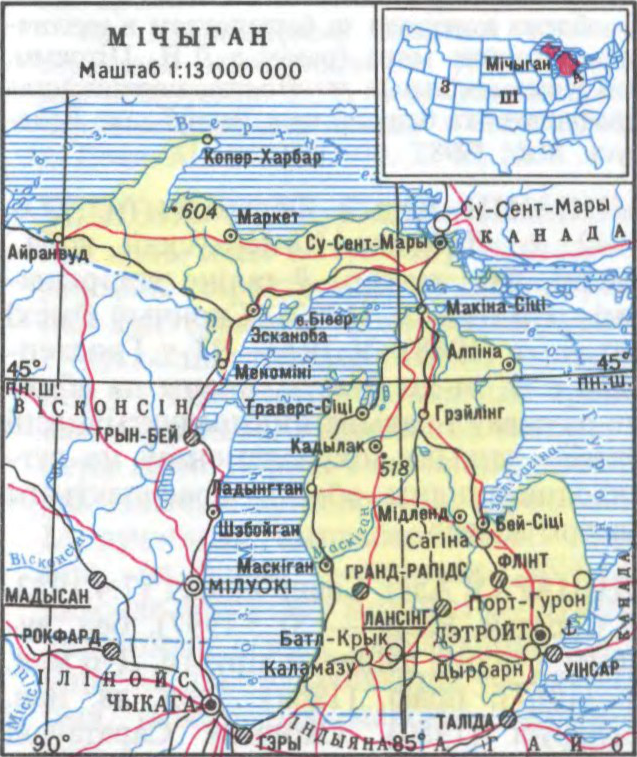
МІ́ЧЫГАН (Michigan),
штат на
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МІ́ЧЫГАН (Michigan),
штат на

Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ГРА́ЗІ ЛЯЧЭ́БНЫЯ,
пелоіды, асадкі вадаёмаў, тарфяныя паклады, вывяржэнні гразевых вулканаў і
Ад 25 да 97% масы гразей лячэбных складае гразевы раствор — вытворнае вады ці рапы, мінералізацыя якога ад 0,01
Я.В.Малашэвіч.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
КІСЛО́ТЫ,
клас
У залежнасці ад колькасці іонаў вадароду, што адшчапляюцца ад малекулы, К. падзяляюць на аднаасноўныя (
Літ.:
Усанович М.И. Исследования в области теории растворов и теории кислот и оснований: Избр.
Мискиджьян С.П., Гарновский А.Д. Введение в современную теорию кислот и оснований. Киев, 1979.
В.В.Свірыдаў.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
КРОЎ,
вадкая тканка, што цыркулюе ў крывяноснай сістэме чалавека, пазваночных жывёл і некат. беспазваночных (
К. у чалавека складае 5—8% яго масы. У яе саставе вадкая частка — плазма (55%), у якой раствораны бялкі, тлушчы, тлушчападобныя рэчывы, вугляводы,
Літ.:
Кассирский И.А., Алексее в Г.А. Клиническая гематология. 4 изд.
Л.У.Чантурыя.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ЛІ́ТЫЙ (
Li, хімічны элемент I
Мяккі і пластычны серабрыста-беды метал,
І.В.Боднар.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МЕТАЛААРГАНІ́ЧНЫЯ ЗЛУЧЭ́ННІ,
злучэнні, у малекулах якіх ёсць сувязь метал—вуглярод (M—C);
Фіз. ўласцівасці М.з. непераходных металаў залежаць ад характару сувязі метал—вуглярод. М.з. шчолачных і шчолачназямельных металаў (за выключэннем літыйарганічных злучэнняў і магнійарганічных злучэнняў, злучэнні з іоннай сувяззю M—C) —
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МІНЕРА́ЛЬНЫ АБМЕ́Н,
сукупнасць працэсаў ужывання, усмоктвання, размеркавання і выдзялення неарганічных рэчываў з арганізма жывёл і чалавека. Разам з водным абменам М.а. забяспечвае пастаянства асматычнай канцэнтрацыі, іоннага складу, кіслотна-шчолачнай раўнавагі, аб’ёму вадкасцей
Літ.:
Гинецинский А.Г. Физиологические механизмы водно-солевого равновесия.
Кравчинский Б.Д. Физиология водно-солевого обмена жидкостей тела.
С.С.Ермакова.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
НІ́КЕЛЬ (
Ni, хімічны элемент VIII групы
Серабрыста-белы коўкі метал, tпл 1455
У.С.Камароў.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
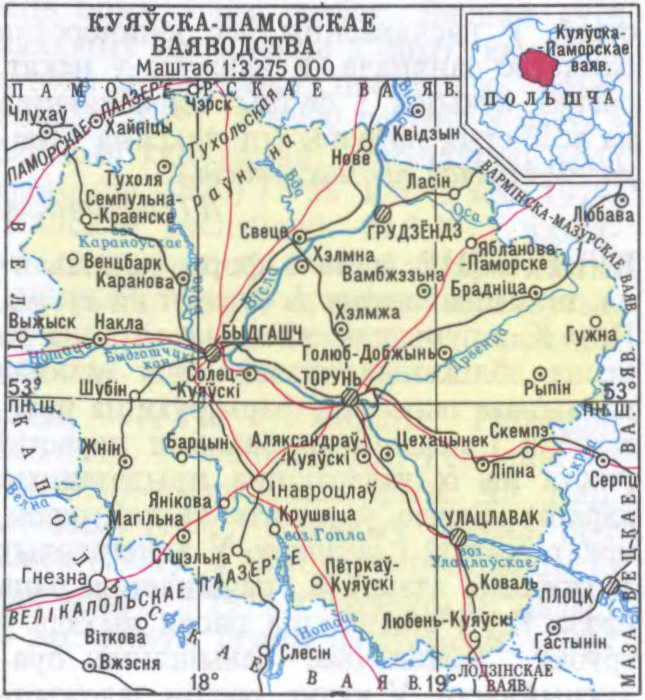
КУЯ́ЎСКА-ПАМО́РСКАЕ ВАЯВО́ДСТВА (Województwo Kujawsko-Pomorskie),
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МА́РГАНЕЦ (
Серабрыста-белы метал, tпл 1244
А.П.Чарнякова.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)