ЗНА́КІ ХІМІ́ЧНЫЯ,
скарочаныя
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ЗНА́КІ ХІМІ́ЧНЫЯ,
скарочаныя
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
НАВУМАВЕ́Ц (Антон Рыгоравіч) (
украінскі фізік.
Тв.:
Двумерные кристаллы. Киев, 1988 (разам з І.Ф.Люксютавым, В.Л.Пакроўскім).
М.П.Савік.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
КЕ́НАН ((Kennan) Джордж Фрост) (
амерыканскі дыпламат, саветолаг. Скончыў
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МАРСКІ́ ТРА́НСПАРТ,
адзін з
М.т. вядомы ў
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
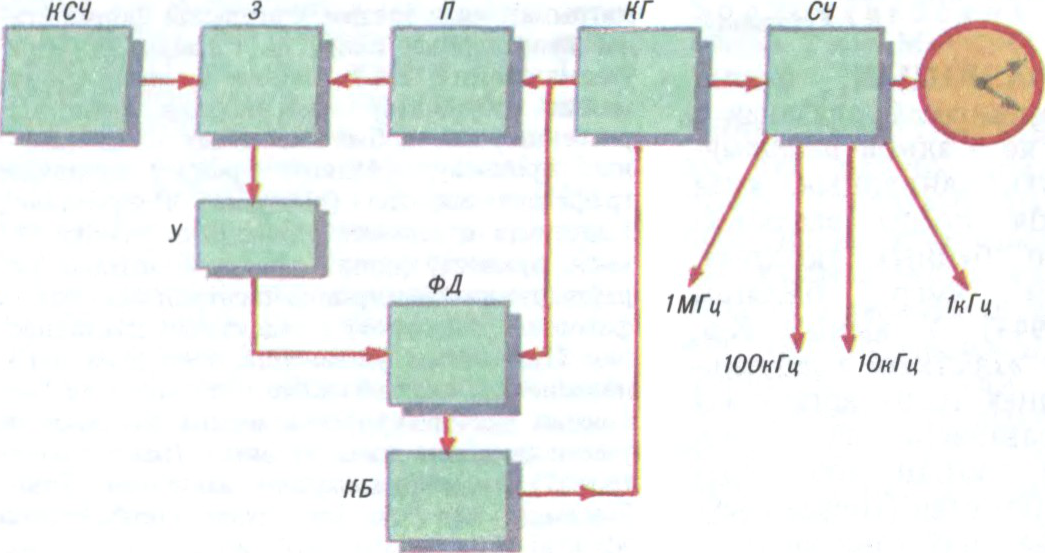
КВА́НТАВЫ ГАДЗІ́ННІК,
прылада для дакладнага вымярэння часу, якая мае кварцавы генератар, што кіруецца квантавым стандартам частаты. Ход К.г. рэгулюе частата выпрамянення атамаў або малекул пры іх квантавых пераходах з аднаго
Гэтая частата настолькі стабільная (хібнасць 10−11—10−13), што дазваляе вымяраць час больш дакладна, чым з выкарыстаннем
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
КРЭ́ЙСЕР (галанд. kruiser ад kruisen плаваць морам),
баявы карабель для пошуку і знішчэння падводных лодак, надводных караблёў (суднаў), берагавых аб’ектаў праціўніка, вядзення бою ў складзе злучэнняў, забеспячэння высадкі марскіх дэсантаў, устаноўкі мінных загарод і
Развіўся з ветразевых фрэгатаў і карветаў. Як клас караблёў ваенных упершыню з’явіўся ў 1860-я
Літ.:
Шершов А.П. История военного кораблестроения с древнейших времен и до наших дней. СПб., 1994;
Энциклопедия кораблей. СПб.,
У.Я.Калаткоў.

Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
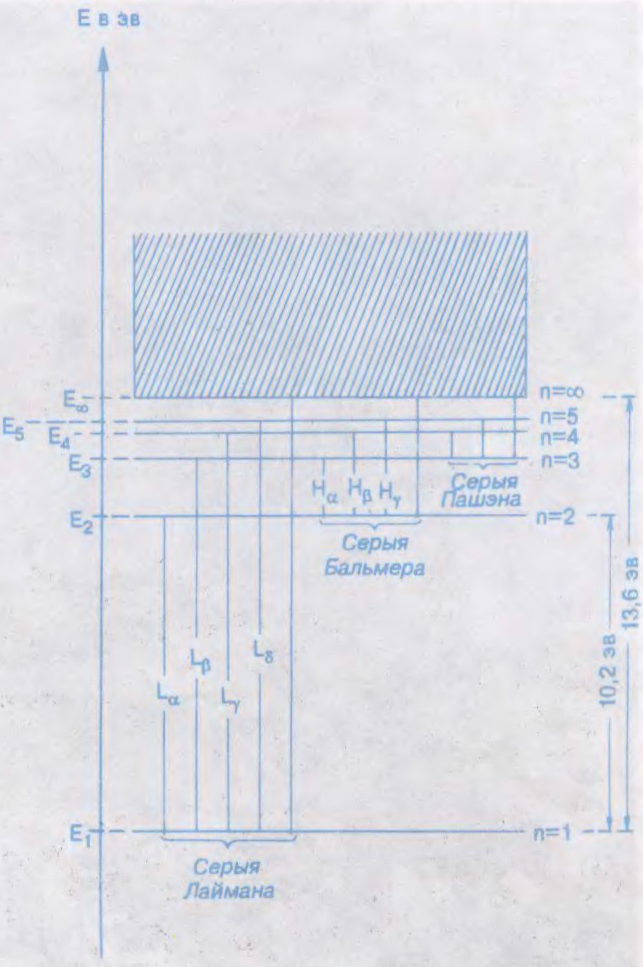
А́ТАМНЫЯ СПЕ́КТРЫ,
спектры, якія ўзнікаюць пры выпрамяненні і паглынанні фатонаў свабоднымі ці слаба ўзаемадзейнымі атамамі (атамнымі газамі, парай невял. шчыльнасці). Лінейчастыя, складаюцца з асобных спектральных ліній, кожная з якіх адпавядае пераходу электрона паміж двума адпаведнымі ўзроўнямі энергіі атама.
Спектральныя лініі характарызуюцца пэўнымі значэннямі частаты ваганняў святла ν, хвалевага ліку ν/c і даўжыні хвалі , дзе c — скорасць святла ў вакууме. Для найбольш простых атамных спектраў, якімі з’яўляюцца спектры атама вадароду і вадародападобных іонаў, месцазнаходжанне спектральных ліній вызначаецца па формуле:
, дзе En — энергія ўзроўню, h — Планка пастаянная, R — Рыдберга пастаянная, Z —
Тэорыя атамных спектраў заснавана на характарыстыцы электронаў у атаме квантавымі лікамі n і 1 і дазваляе вызначыць магчымыя ўзроўні энергіі. Вывучаны спектры
Літ.:
Ельяшевич М.А. Атомная и молекулярная спектроскоп я.
Фриш С.Э. Оптические спектры атомов
Собельман И.И. Введение в теорию атомных спектров.
М.А.Ельяшэвіч.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
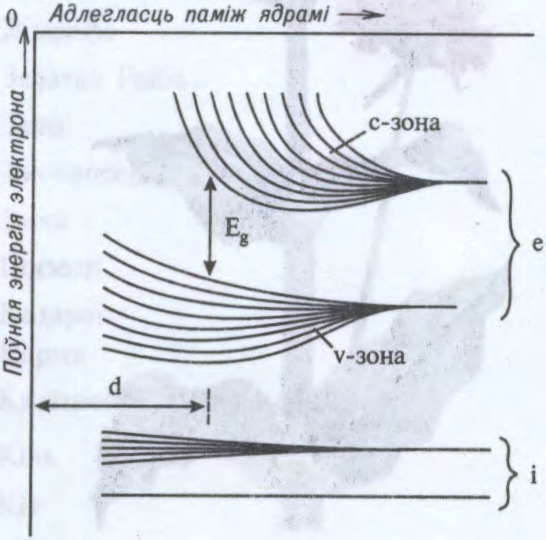
ЗО́ННАЯ ТЭО́РЫЯ
квантавая тэорыя спектра энергій электронаў крышталя. Паводле З.т. гэты спектр складаецца з зон дазволеных і забароненых энергій. З.т. тлумачыць шэраг уласцівасцей і з’яў у крышталях, у прыватнасці, розны характар іх электраправоднасці.
Аснова З.т. — аднаэлектроннае прыбліжэнне: скорасць руху атамных ядраў каля становішчаў раўнавагі многа меншая за скорасць электронаў; кожны электрон рухаецца ў трохмерна-перыядычным полі, якое ствараецца ядрамі і астатнімі электронамі. Зона праводнасці (с) і валентная зона (v) утвораны сукупнасцю атамных
Літ.:
Харрисон У.А. Электронная структура и свойства твердых тел: Физика химической связи:
Анималу А. Квантовая теория кристаллических твердых тел:
М.А.Паклонскі.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
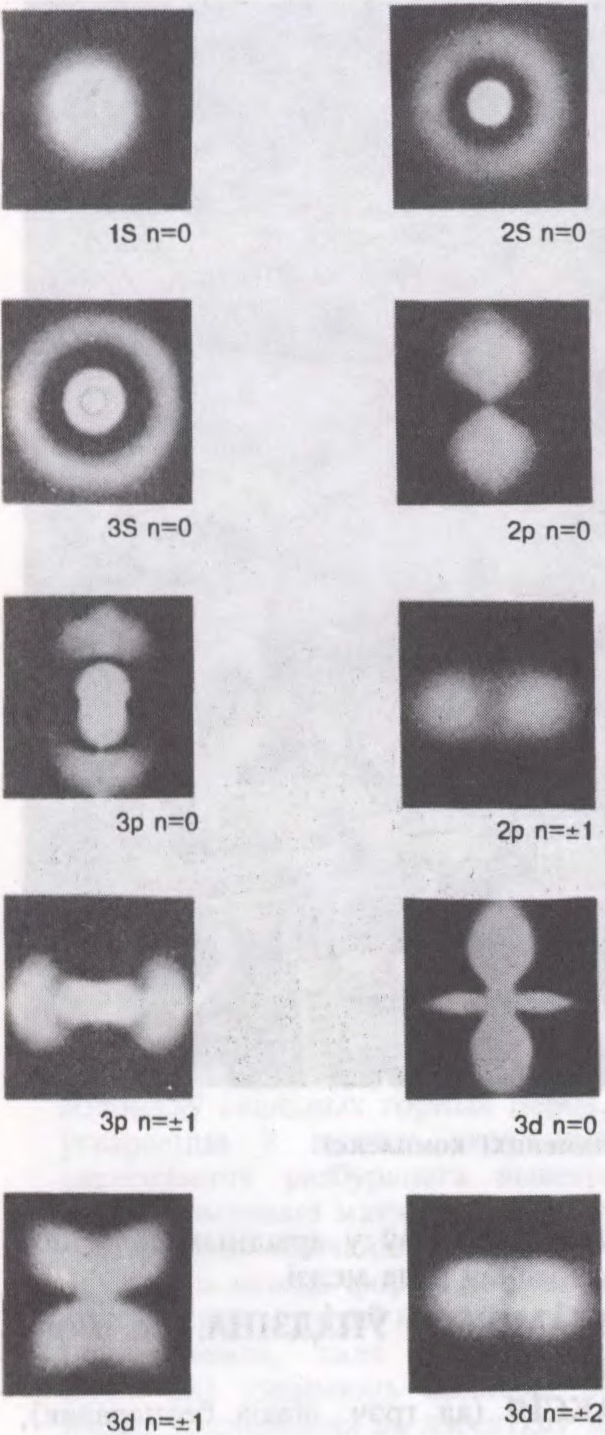
А́ТАМ (ад
часціца рэчыва, найменшая частка
Літ.:
Шпольский Э.В. Атомная физика.
Борн М. Атомная физика.
Гольдин Л.Л., Новикова Г.И. Введение в квантовую физику.
Ландау Л.Д., Лифшиц Е.М. Теоретическая физика.
Нерелятивистская теория. 4 изд.
М.А.Ельяшэвіч.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
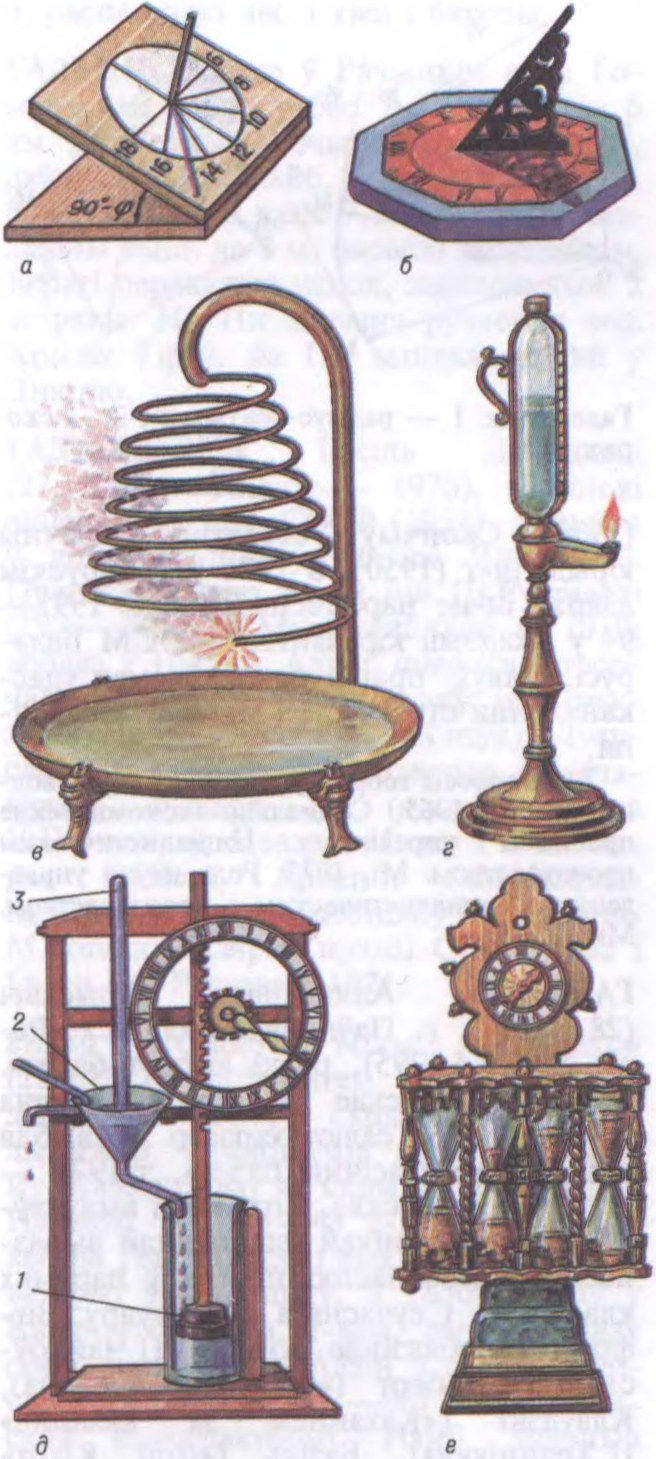
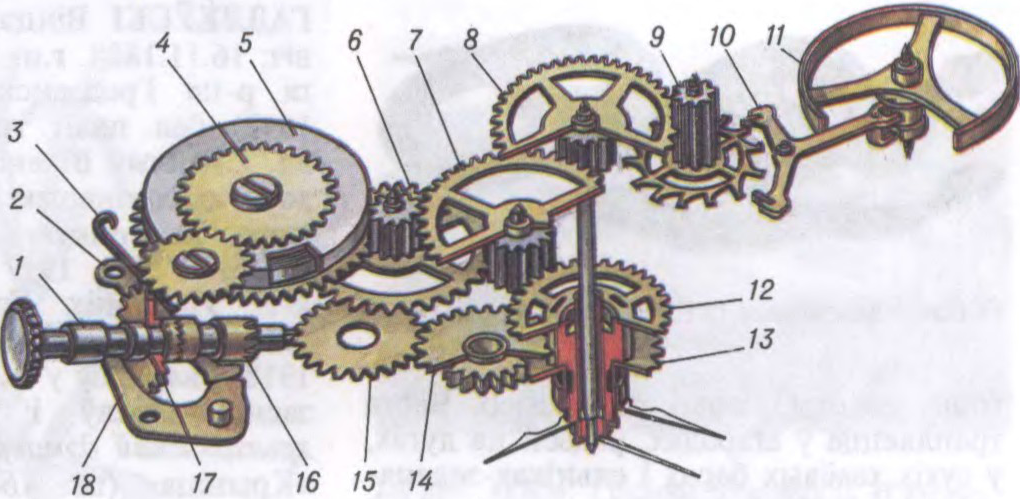
ГАДЗІ́ННІК,
прылада для вымярэння часу. Бываюць: сонечныя, вадзяныя, пясочныя, агнявыя, механічныя, электрычныя (
На Беларусі унікальным помнікам сярэдневяковай тэхнікі з’яўляецца вежавы гадзіннік касцёла езуітаў у Гродне, створаны ў 2-й
Літ.:
Пипуныров В.Н. История часов с древнейших времен до наших дней.
Завельский Ф.С. Время и его измерение. 5 изд.
Шполянский В.А., Чернягин Б.М. Электрические приборы времени.
Мясников Л.Л., Булыгин А.С. Атомные часы и система времени.
У.М.Сацута.

Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)