ВАЛЮ́ТНАЯ СІСТЭ́МА,
сукупнасць грашова-крэдытных адносін, што склаліся на аснове інтэрнацыяналізацыі
З 19
Г.І.Краўцова.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ВАЛЮ́ТНАЯ СІСТЭ́МА,
сукупнасць грашова-крэдытных адносін, што склаліся на аснове інтэрнацыяналізацыі
З 19
Г.І.Краўцова.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
АСТРАНАМІ́ЧНЫЯ ІНСТРУМЕ́НТЫ І ПРЫЛА́ДЫ,
оптыка-механічная і электронная апаратура для астранамічных назіранняў і апрацоўкі іх даных. Дапамагаюць вызначаць становішча
Найбольш
Літ.:
Курс астрофизики и звездной астрономии.
Мартынов Д.Я. Курс практической астрофизики.
М.М.Міхельсон.





Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
А́ТАМНЫЯ СПЕ́КТРЫ,
спектры, якія ўзнікаюць пры выпрамяненні і паглынанні фатонаў свабоднымі ці слаба ўзаемадзейнымі атамамі (атамнымі газамі, парай невял. шчыльнасці). Лінейчастыя, складаюцца з асобных спектральных ліній, кожная з якіх адпавядае пераходу электрона паміж двума адпаведнымі ўзроўнямі энергіі атама.
Спектральныя лініі характарызуюцца пэўнымі значэннямі частаты ваганняў святла ν, хвалевага ліку ν/c і даўжыні хвалі , дзе c — скорасць святла ў вакууме. Для найбольш простых атамных спектраў, якімі з’яўляюцца спектры атама вадароду і вадародападобных іонаў, месцазнаходжанне спектральных ліній вызначаецца па формуле:
, дзе En — энергія ўзроўню, h — Планка пастаянная, R — Рыдберга пастаянная, Z — атамны нумар, n — галоўны квантавы лік. Спектральныя лініі аб’ядноўваюцца ў спектральныя серыі, адна з якіх (пры , )
Тэорыя атамных спектраў заснавана на характарыстыцы электронаў у атаме квантавымі лікамі n і 1 і дазваляе вызначыць магчымыя ўзроўні энергіі. Вывучаны спектры
Літ.:
Ельяшевич М.А. Атомная и молекулярная спектроскоп я.
Фриш С.Э. Оптические спектры атомов
Собельман И.И. Введение в теорию атомных спектров.
М.А.Ельяшэвіч.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ГІДРАІЗАЛЯЦЫ́ЙНЫЯ МАТЭРЫЯ́ЛЫ,
матэрыялы для аховы (гідраізаляцыі)
Абклеечныя гідраізаляцыйныя матэрыялы — руберойд, пергамін, гідраізол, шклоруберойд, металаізол і
А.Я.Вакар.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ЛІТАЛО́ГІЯ (ад літа... + ...логія),
навука пра асадкавыя горныя пароды і сучасныя асадкі. Вывучае іх рэчыўны
Л. склалася як адна з галін геалогіі ў канцы 19 —
На Беларусі вывучэнне асадкавых парод вядзецца з
Літ.:
Фролов В.Т. Литология.
Систематика и классификации осадочных пород и их аналогов. СПб., 1998.
М.В.Вераценнікаў.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МЕ́ДЗІ ЗЛУЧЭ́ННІ,
хімічныя злучэнні, у
А.П.Чарнякова.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МЕТАЛАЗНА́ЎСТВА,
навука пра
М. развіваецца з 2-й
На Беларусі работы ў галіне М. вядуцца ў Ін-це фізікі цвёрдага цела і паўправаднікоў, Фізіка-
Літ.:
Бочвар А.А. Металловедение. 5 изд.
Болховитинов Н.Ф. Металловедение и термическая обработка. 6 изд.
Структура и свойства металлов и сплавов.
А.П.Ласкаўнёў.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МЫШ’ЯКУ́ ЗЛУЧЭ́ННІ,
хімічныя злучэнні, у
А.П.Чарнякова.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
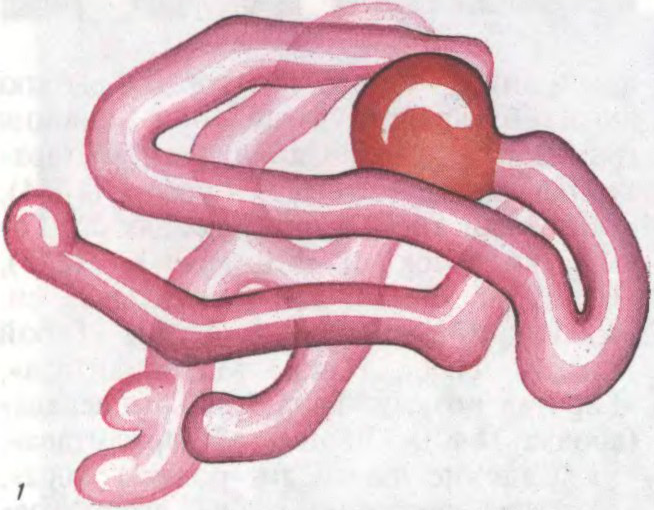
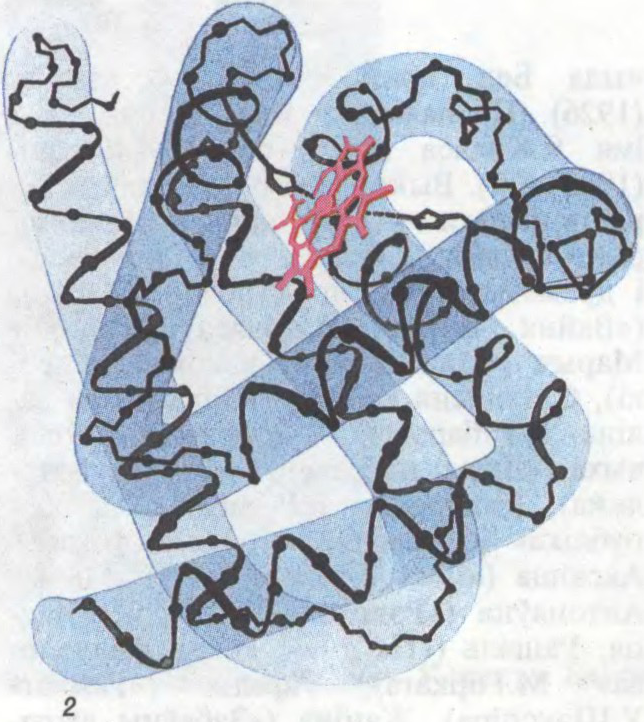
БЯЛКІ́,
прыродныя высокамалекулярныя
Агульны
Літ.:
Бохински Р. Современные воззрения в биохимии:
Ленинджер А. Основы биохимии:
Гершкович А.А. От структуры к синтезу белка. Киев, 1989;
Овчинников Ю.А. Химия жизни: Избр.
У.М.Рашэтнікаў.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
БА́РЫЮ ЗЛУЧЭ́ННІ,
хімічныя злучэнні, у
Літ.:
Ахметов Т.Г. Химия и технология соединений бария.
Л.М.Скрыпнічэнка.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)