МА́ГМА (
расплаўленая, пераважна сілікатная маса, што ўзнікае ў зямной кары або верхняй мантыі Зямлі. У растворы М. прысутнічаюць злучэнні
Р.Р.Паўлавец.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МА́ГМА (
расплаўленая, пераважна сілікатная маса, што ўзнікае ў зямной кары або верхняй мантыі Зямлі. У растворы М. прысутнічаюць злучэнні
Р.Р.Паўлавец.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ПАВЕ́ТРА,
сумесь газаў, што ўтвараюць атмасферу Зямлі.
Састаў П. (у працэнтах па аб’ёме); азот — 78,09, кісларод — 20,95, аргон — 0,932, дыаксід вугляроду — 0,032, гелій, крыптон, неон,
На Беларусі
Л.М.Скрыпнічэнка.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ПА́ЛІВА,
рэчывы, якія пры спальванні вылучаюць значную колькасць цеплаты і выкарыстоўваюцца для атрымання цеплавой энергіі. Паводле паходжання падзяляюць на прыроднае (антрацыт, буры вугаль, газы прыродныя гаручыя, гаручыя сланцы, драўніна, каменны вугаль, нафта, торф) і штучнае (
Уласцівасці П. ў значнай ступені абумоўлены яго
Л.М.Скрыпнічэнка.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
аднаві́ць, ‑наўлю, ‑новіш, ‑новіць;
1. Вярнуць да ранейшага стану, выгляду што‑н. пашкоджанае, парушанае, заняпалае; адрадзіць; узнавіць.
2.
3. Вярнуць каму‑н. ранейшае службовае ці прававое становішча.
4. Пачаць зноў перарванае дзеянне, адносіны.
5. Выдзеліць з хімічных злучэнняў кісларод і далучыць
Тлумачальны слоўнік беларускай мовы (1977-84, правапіс да 2008 г.)
БРОМ (
Br, хімічны элемент VII групы
Бром — чырвона-бурая вадкасць з непрыемным рэзкім пахам, лёгка выпараецца, tпл -7,25
Літ.:
Ксензенко В.И., Стасиневич Д.С. Химия и технология брома, йода и их соединений.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ПАЛА́ДЫЙ (
Pd, хімічны элемент VIII групы
Серабрыста-белы мяккі метал, tпл 1554
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
злучы́ць
1.
2.
Беларуска-рускі слоўнік, 4-е выданне (2012, актуальны правапіс)
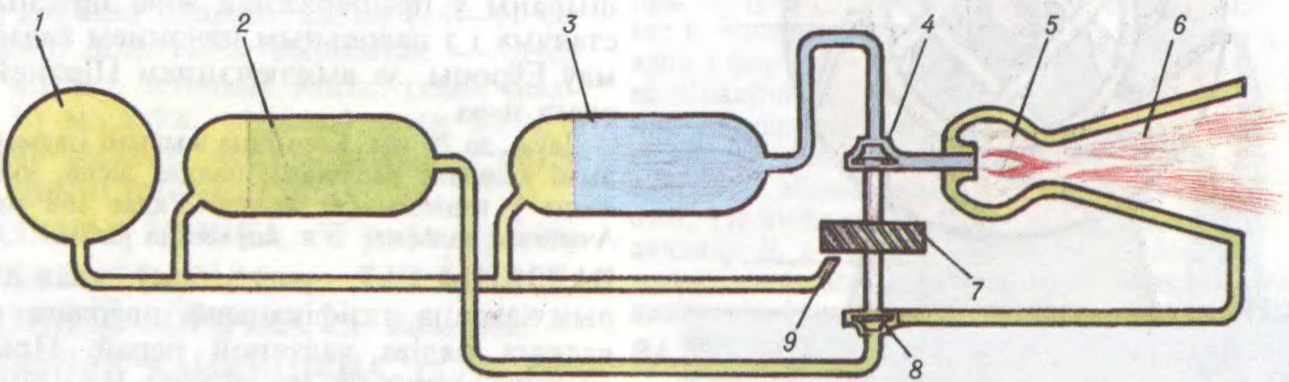
ВА́ДКАСНЫ РАКЕ́ТНЫ РУХАВІ́К,
ракетны рухавік, які працуе на вадкім паліве;
Складаецца з камеры згарання, рэактыўнага сапла, сістэм сілкавання, рэгулявання падачы і ўзгарання паліва і дапаможных агрэгатаў. Сістэма сілкавання палівам — выцясняльная (газабалонная) ці турбапомпавая. Гаручае і акісляльнік змешваюцца і ўзгараюцца ў камеры, адкуль газавы струмень праз сапло з
Літ.:
Бычков В.Н., Назаров Г.А., Прищепа В.Н. Космические жидкостноракетные двигатели.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
АКІСЛЕ́ННЕ-АДНАЎЛЕ́ННЕ,
хімічныя рэакцыі, пры якіх адбываецца пераход электронаў ад атамаў, малекул ці іонаў аднаго злучэння да атамаў, малекул і іонаў другога. Паводле электроннай тэорыі акісленне вызначаецца як страта (
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МАЛАКО́,
сакраторная вадкасць малочных залоз млекакормячых жывёл і чалавека, фізіялагічна прызначаная для выкормлівання дзіцянят. Выпрацоўваецца ў перыяд лактацыі. Змяшчае большасць элементаў, неабходных для нармальнага росту і развіцця арганізма, аховы яго ад захворванняў, у збалансаваным, аптымальным для засваення стане. Склад М. залежыць ад віду, пароды, узросту жывёл, стадыі лактацыі, сезона года і
Л.Л.Галубкова.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)