НО́ВАЯ ШАТЛА́НДЫЯ (
правінцыя на
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
НО́ВАЯ ШАТЛА́НДЫЯ (
правінцыя на
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
О́НІЕВЫЯ ЗЛУЧЭ́ННІ,
арганічныя злучэнні іоннага характару агульнай ф-лы [Rn+1Э]+X −, дзе R —
Стабільныя О.з. — цвёрдыя солепадобныя рэчывы, раствараюцца ў вадзе і палярных
Л.М.Скрыпнічэнка.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
БА́РЫЮ ЗЛУЧЭ́ННІ,
хімічныя злучэнні, у састаў якіх уваходзіць барый, пераважна ў ступені акіслення +2.
Літ.:
Ахметов Т.Г. Химия и технология соединений бария.
Л.М.Скрыпнічэнка.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ГАЛУРГІ́Я (ад гала... +
галіна
На Беларусі даследаванні па галургіі праводзяцца ў Ін-це агульнай і неарган. хіміі
Літ.:
Галургия: Теория и практика.
М.І.Вараб’ёў.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
БО́РНАЯ КІСЛАТА́,
слабая неарганічная кіслата (H3BO3). Бясколерныя крышталі,
У прыродзе існуе як мінерал сасалін, а таксама ў тэрмальных водах і прыродных расолах, з якіх яе атрымліваюць. Вышэй за 70
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
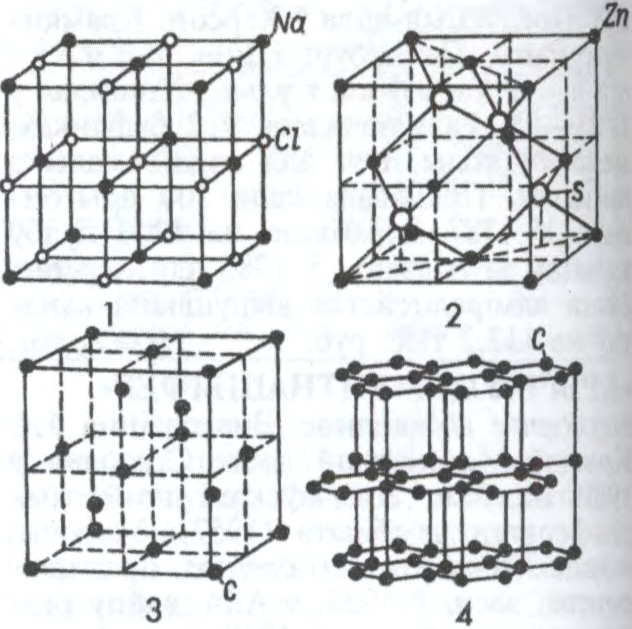
КРЫШТАЛІ́ЧНАЯ РАШО́ТКА рэгулярнае размяшчэнне часціц (атамаў, іонаў, малекул) у крышталях, якое характарызуецца перыядычнай паўтаральнасцю ў трох вымярэннях. Для апісання К.р. дастаткова ведаць размяшчэнне часціц
У адпаведнасці з сіметрыяй крышталя элементарная ячэйка мае форму паралелепіпеда ці прызмы; памеры рэбраў
Р.М.Шахлевіч.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
КУЛУНДЗІ́НСКАЯ РАЎНІ́НА,
раўніна на
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МЕРКАПТА́НЫ [ад
Аліфатычныя
Я.Г.Міляшкевіч.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
НІТРАВА́ННЕ,
хімічная рэакцыя ўвядзення нітрагрупы — NO2 у малекулу
Адбываецца. ў выніку замяшчэння атамаў вадароду (прамое Н.) ці
Я.Г.Міляшкевіч.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ПАКО́СТЫ (ад польскага pokost лак),
вадкія плёнкаўтваральныя рэчывы на аснове алеяў ці алкідных смол. Колер ад жоўтага да вішнёвага. Добра змочваюць металы, дрэва, тканіну. Нанесеныя тонкім слоем высыхаюць пры пакаёвай т-ры за 24
Адрозніваюць натуральныя, камбінаваныя, паўнатуральныя (
Л.М.Скрыпнічэнка.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)