Беларуская Савецкая Энцыклапедыя (1969—76, паказальнікі; правапіс да 2008 г., часткова)
Verbum
анлайнавы слоўнікчасціца рэчыва, найменшая частка
Літ.:
Шпольский Э.В. Атомная физика.
Борн М. Атомная физика.
Гольдин Л.Л., Новикова Г.И. Введение в квантовую физику.
Ландау Л.Д., Лифшиц Е.М. Теоретическая физика.
Нерелятивистская теория. 4 изд.
М.А.Ельяшэвіч.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
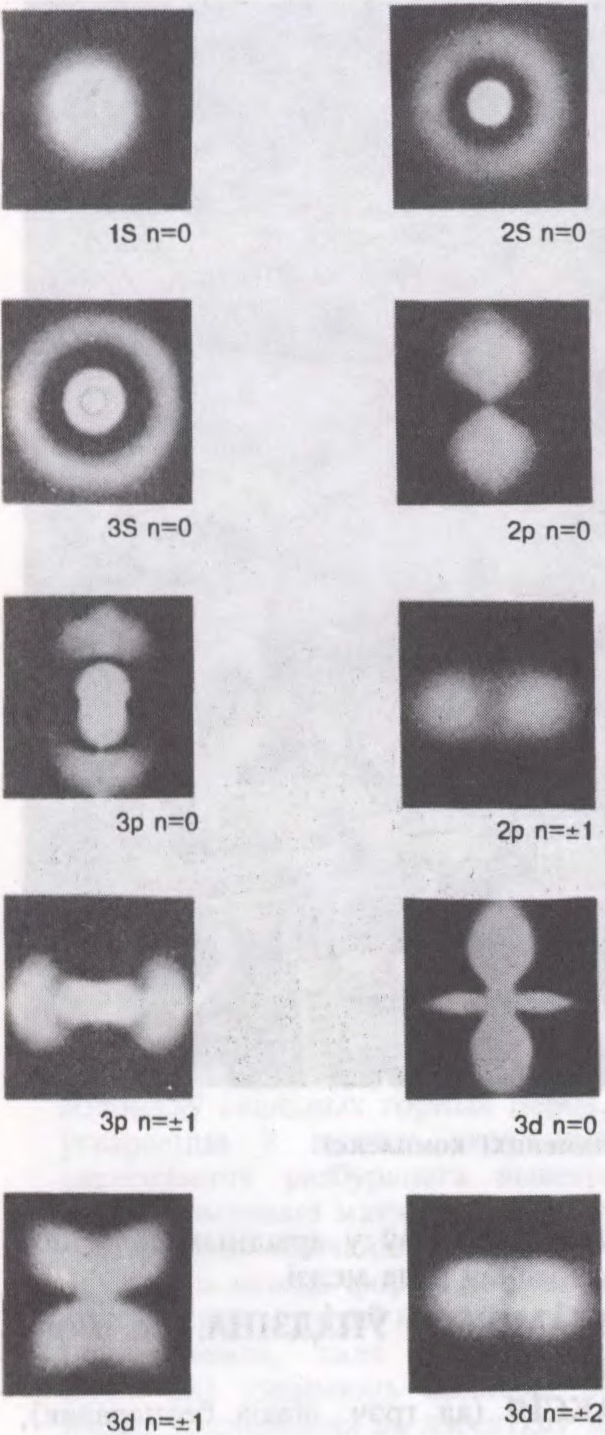
ВАДАРОДАПАДО́БНЫЯ А́ТАМЫ,
1) іоны лёгкіх элементаў, якія, як вадарод, маюць ядро і адзін электрон.
2) Нестабільныя часціцы,
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
АТАМІ́СТЫКА,
вучэнне пра дыскрэтную (перарыўную) будову матэрыі. Узнікла ў антычнай філасофіі. Адзін з яе стваральнікаў Дэмакрыт сцвярджаў, што першапачаткам усяго існага з’яўляюцца атамы (быццё) і пустата (небыццё).
Т.І.Адула.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
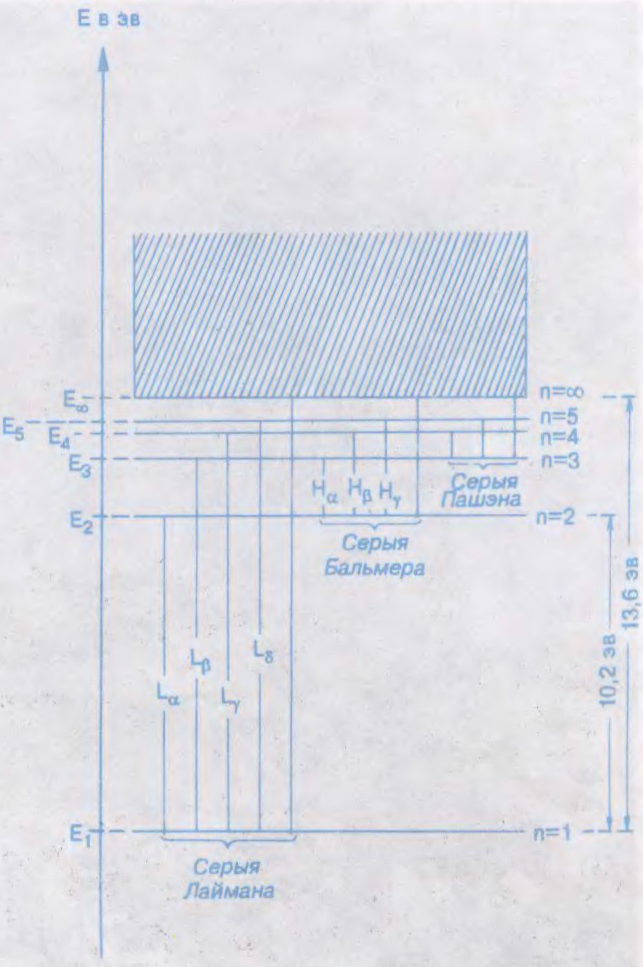
КВАНТ ЭНЕ́РГІІ,
вызначаная колькасць энергіі, якую можа вылучыць ці паглынуць мікрасістэма (атамнае ядро,
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ДО́НАР
дэфект
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
КРЭМНІЙАРГАНІ́ЧНЫЯ ЗЛУЧЭ́ННІ,
рэчывы, малекулы якіх маюць атамы крэмнію (Si), злучаныя з атамам вугляроду непасрэдна або праз
Вядомы розныя групы
Я.Г.Міляшкевіч.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МА́САВЫ ЛІК,
колькасць нуклонаў (пратонаў і нейтронаў) у атамным ядры. Абазначаецца A і звычайна паказваецца індэксам уверсе злева ад сімвала
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
І́РНШАЎ ТЭАРЭ́МА,
адна з
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ВАЛЕ́НТНАСЦЬ (ад
здольнасць атама
Валентнасць вызначаецца толькі колькасцю кавалентных сувязяў. Для злучэнняў з іоннай сувяззю выкарыстоўваецца паняцце акіслення ступень, якая колькасна роўная валентнасці, але дадаткова характарызуецца дадатным ці адмоўным знакам. У комплексных злучэннях і іонных крышталях каардынацыйны лік атамаў (іонаў) перавышае велічыню спін-валентнасці, таму карыстаюцца паняццем каардынацыйнай валентнасці, якая колькасна роўная суме спін-валентнасці і колькасці атамаў (іонаў), дадаткова звязаных з валентнанасычаным атамам.
Літ.:
Чаркин О.П. Проблемы теории валентности, химической связи, молекулярной структуры.
В.В.Свірыдаў.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)