АРБАРЫЦЫ́ДЫ [ад
хімічныя рэчывы, якія знішчаюць дрэвавую расліннасць і хмызнякі. Арбарыцыдамі з’яўляюцца эфіры і
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
АРБАРЫЦЫ́ДЫ [ад
хімічныя рэчывы, якія знішчаюць дрэвавую расліннасць і хмызнякі. Арбарыцыдамі з’яўляюцца эфіры і
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
АСНО́ВЫ,
клас
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
АЎТЫГЕ́ННЫЯ МІНЕРА́ЛЫ (ад
мінералы асадкавых горных парод, якія ўтварыліся ў працэсе седыментацыі і літагенезу. Аўтыгеннымі мінераламі з’яўляюцца розныя карбанаты, растваральныя
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ГІДРАСУЛЬФІ́ТЫ,
бісульфіты, гідрагенсульфіты, кіслыя
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
КРЭ́МНІЕВЫЯ КІСЛО́ТЫ,
група
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МАЛО́НАВАЯ КІСЛАТА́,
CH2(COOH)2, двухасноўная кіслата насычанага раду. У свабодным выглядзе прысутнічае ў раслінах: лісці бабовых, зялёных
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
АСА́ДКАВЫЯ ГО́РНЫЯ ПАРО́ДЫ,
горныя пароды, якія ўтвараюцца асаджэннем рэчыва ў водным асяроддзі, радзей з паветра і ў выніку дзейнасці ледавікоў. У залежнасці ад характару асаджэння падзяляюцца на абломкавыя,
Літ.:
Материалы по стратиграфии Белоруссии: (к Межведомств. стратигр. Совещанию, Минск, октябрь, 1981
Логвиненко Н.В. Петрографяя осадочных пород с основами методики исследования. 3 изд.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ГАЛІ́Т (ад
У.Я.Бардон.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
КАНІФО́ЛЬ,
цвёрды прадукт, што застаецца пасля адгонкі шкіпінару са смольных рэчываў драўніны хваёвых парод.
Крохкая, шклопадобная, празрыстая смала светла-жоўтага (часам цёмна-рудога) колеру. Размякчаецца пры т-ры 40—75
Я.Г.Міляшкевіч.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
КАРБАНА́ТЫ,
К. 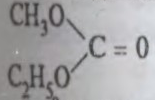 метылэтылкарбанат, tкіп 107
метылэтылкарбанат, tкіп 107
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)