НІ́ЗКІЯ ТЭМПЕРАТУ́РЫ.
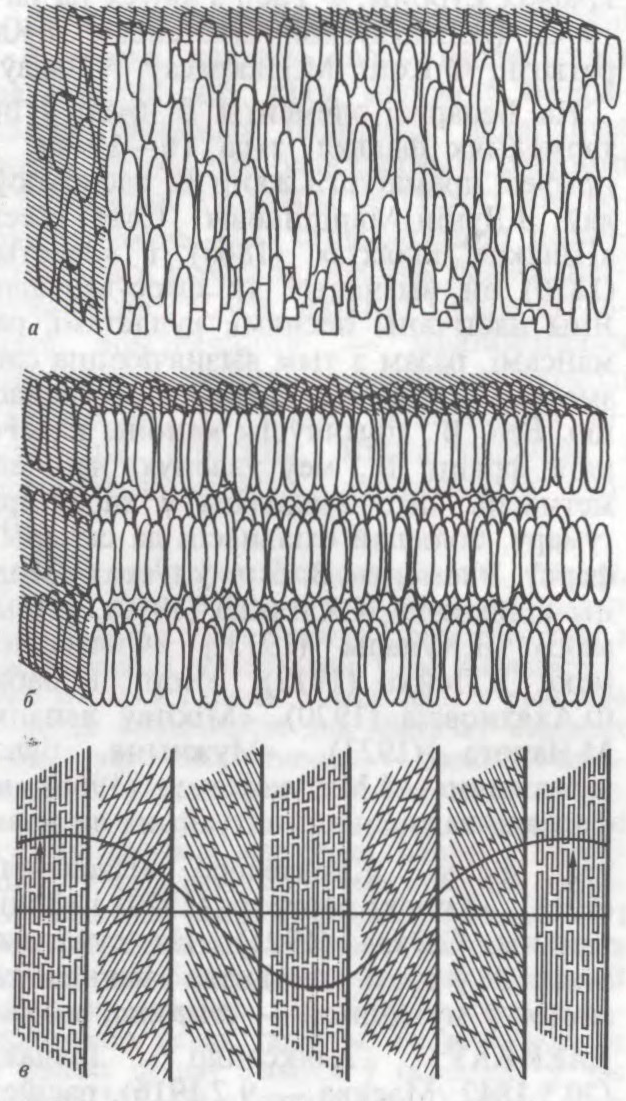
крыягенныя тэмпературы, тэмпературы ніжэй за 120 К. Т-ры. меншыя за 0,3 К, адносяць да звышнізкіх. Пры Н.т., асабліва блізкіх да абсалютнага нуля, цеплавы рух атамаў рэчыва памяншаецца і пачынаюць праяўляцца яго квантавыя ўласцівасці (напр., звышправоднасць, звышцякучасць). Пры Н.т. стан цвёрдага рэчыва разглядаецца як упарадкаваны, што дазваляе апісваць яго ўласцівасці з дапамогай квазічасціц. Кандэнсаваны (вадкі або цвёрды) стан рэчыва пры Н.т. вывучае фізіка нізкіх тэмператур. Эфекты, што праяўляюцца пры Н.т., выкарыстоўваюць у касм. матэрыялазнаўстве, крыябіялогіі, крыяэлектроніцы і інш.
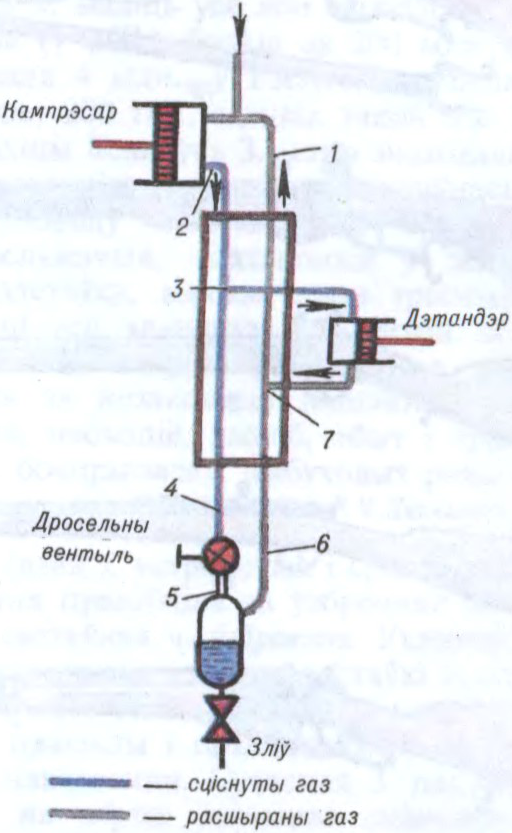
Атрыманне Н. т. заснавана на звадкаванні газаў у спец. устаноўках — звадкавальніках, дзе моцна сціснуты газ пры расшырэнні да звычайнага ціску ахаладжаецца і кандэнсуецца (паводле Джоўля—Тамсана эфекту). Як холадаагенты выкарыстоўваюць паветра, азот, неон, вадарод, гелій (т-ра кіпення Тн = 4,2 К). Для падтрымання Н.т. Тн холадаагента павінна быць пастаяннай пад атм. ціскам, для чаго выкарыстоўваюць спец. тэрмастаты. Адпампоўваннем газу, што выпараецца, з герметызаванай пасудзіны памяншаюць ціск над вадкасцю і гэтым зніжаюць т-ру яе кіпення. Так дасягаюцца Н.т.: ад 77 да 63 К пры дапамозе вадкага азоту, ад 27 да 24 К — вадкага неону, ад 20 да 14 К — вадкага вадароду, ад 4,2 да 1 К — вадкага гелію. Пры больш нізкіх т-рах вадкія газы цвярдзеюць і страчваюць ахаладжальныя якасці (за выключэннем ізатопа гелію 4Не, які застаецца вадкім амаль да абс. нуля). Метадам адыябатычнага размарожвання парамагнітных солей дасягаюць т-ры 10−3 К, гэтым жа метадам з выкарыстаннем ядзернага парамагнітнага рэзанансу ў сістэме атамных ядраў дасягнута т-ра 10−6 К. Т-ры парадку 10−3 К атрымліваюць таксама больш зручным метадам — растварэннем вадкага 3Не у вадкім 4Не. Вымярэнне Н.т. да 1 К ажыццяўляюць газавым тэрмометрам. У дыяпазоне 0,3—5,2 К нізкатэмпературная тэрмаметрыя засн. на залежнасці ціску насычаных пароў гелію ад т-ры. У практычнай тэрмаметрыі выкарыстоўваюць пераважна тэрмометры супраціўлення.
На Беларусі даследаванні з выкарыстаннем Н.т. вядуцца з 1964 у Ін-це фізікі цвёрдага цела і паўправаднікоў, з 1980-х г. — у Цэнтры крыягенных даследаванняў пры гэтым ін-це (В.І.Гасцішчаў, С.Я.Дзям’янаў і інш.), а таксама ў інш. ін-тах Нац. АН, БДУ.
Літ.:
Лоунасмаа О.В. Принципы и методы получения температур ниже 1 К: Пер. с англ. М., 1977;
Капица П.Л. Физика и техника низких температур: Науч. тр. М., 1989;
Вепшек Я. Измерение низких температур электрическими методами: Пер. с чеш. М. 1980.
С.Я.Дзям’янаў.
т. 11, с. 331