МЛАДАГРАМАТЫ́ЗМ,
адна з плыняў параўнальна-гістарычнага мовазнаўства. Склалася ў Еўропе ў 1870-я
Літ.:
Томсен
Пауль Г. Принципы истории языка:
А.Я.Міхнееіч.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МЛАДАГРАМАТЫ́ЗМ,
адна з плыняў параўнальна-гістарычнага мовазнаўства. Склалася ў Еўропе ў 1870-я
Літ.:
Томсен
Пауль Г. Принципы истории языка:
А.Я.Міхнееіч.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
АЭРАДРО́М (ад аэра... +
тэрыторыя з паветранай прасторай, комплексам збудаванняў і абсталявання, якія прызначаны для ўзлёту, пасадкі, размяшчэння і абслугоўвання самалётаў, верталётаў і планёраў.
Бываюць аэрадромы грамадзянскія, ваенныя і сумеснага базіравання, трасавыя — для эксплуатацыі самалётаў і верталётаў, якія перавозяць па авіялініях пасажыраў, грузы, пошту (да іх належаць усе аэрадромы аэрапортаў) і
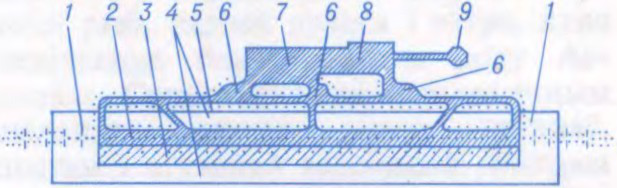
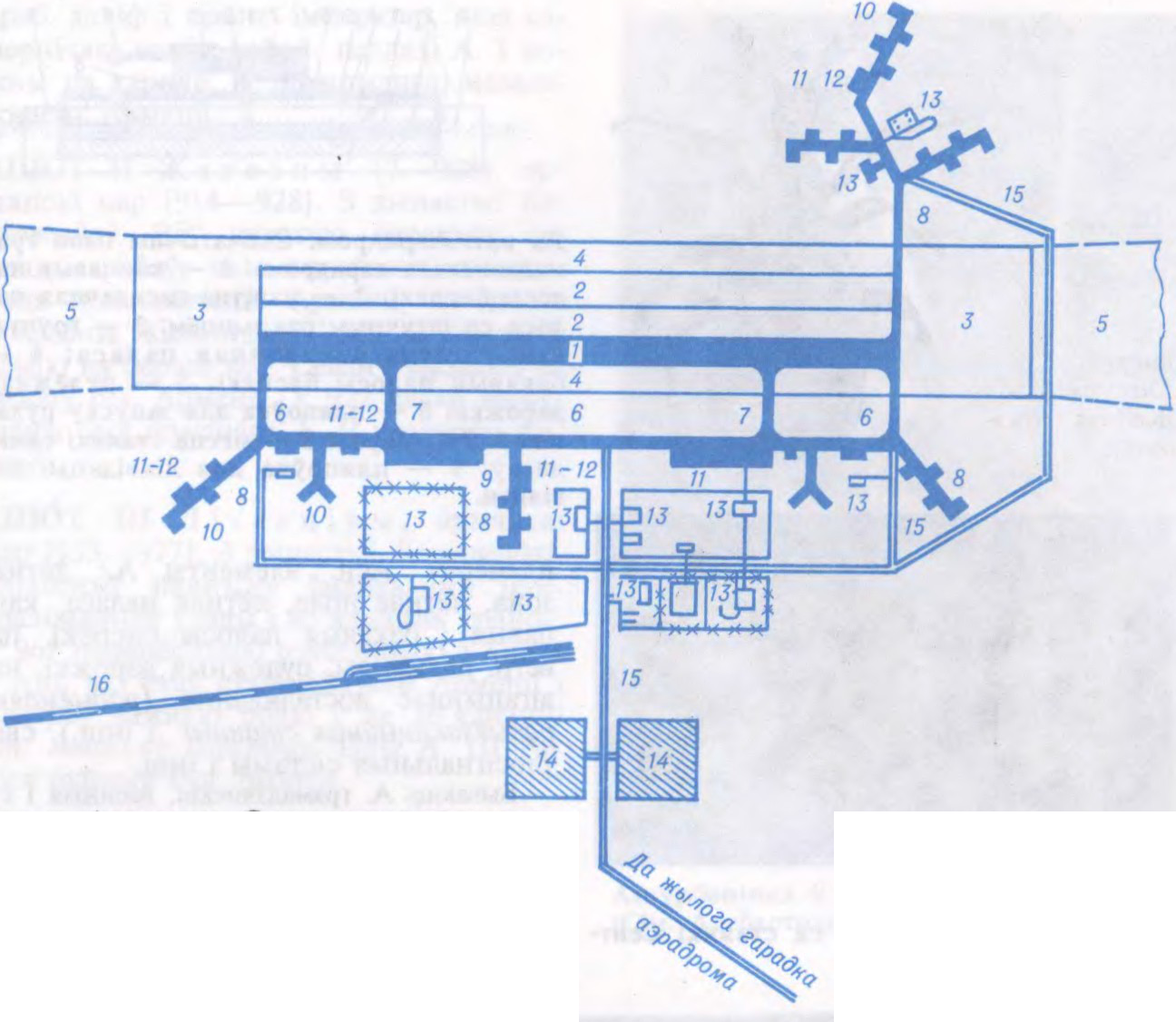
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
БА́РЫЮ ЗЛУЧЭ́ННІ,
хімічныя злучэнні, у састаў якіх уваходзіць барый, пераважна ў
Літ.:
Ахметов Т.Г. Химия и технология соединений бария.
Л.М.Скрыпнічэнка.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
АДСО́РБЦЫЯ (ад
паглынанне рэчыва з газавага або вадкага асяроддзя (адсарбату) паверхняй, мікрасітавінамі цвёрдага цела (адсарбенту) ці вадкасці. Адсорбцыя — прыватны выпадак сорбцыі, якая ўключае абсорбцыю. У аснове адсорбцыі ляжаць асаблівыя ўласцівасці рэчыва ў паверхневым слоі, колькасна яна характарызуецца паверхневым нацяжэннем. Падзяляецца на фізічную абсорбцыю і хемасорбцыю, без рэзкага размежавання паміж імі; часта спалучаецца ў адзіным працэсе.
Велічыню адсорбцыі адносяць да адзінкі паверхні ці масы адсарбенту; яна павялічваецца пры павышэнні канцэнтрацыі адсарбату і памяншаецца пры павышэнні т-ры. Пры цвёрдых адсарбентах велічыню адсорбцыі вызначаюць па колькасці паглынутага рэчыва ці па змене канцэнтрацыі адсарбату; пры вадкіх — па змене паверхневага нацяжэння. Адсорбцыя адыгрывае важную ролю ў цеплаабмене, стабілізацыі калоідных сістэм (
Літ.:
Адамсон А. Физическая химия поверхностей:
Кельцев Н.В. Основы адсорбционной техники. 2 изд.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
АЛЮМІ́НІЮ ЗЛУЧЭ́ННІ,
хімічныя злучэнні, у састаў якіх уваходзіць алюміній, пераважна ў
Л.М.Скрыпнічэнка.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ДРЭ́ВА шматгадовая расліна з выразным, у рознай
Д. ўзніклі ў сярэднім дэвоне. Належаць пераважна да хвойных (з голанасенных) і двухдольных (з пакрытанасенных) раслін. Крона ў большасці Д. складаецца з галін і лісця. Ствол захоўваецца на працягу ўсяго жыцця, кожны год дае прырост у таўшчыню, утвараючы гадавыя кольцы. У Д. з класа аднадольных (
Выкарыстоўваецца са
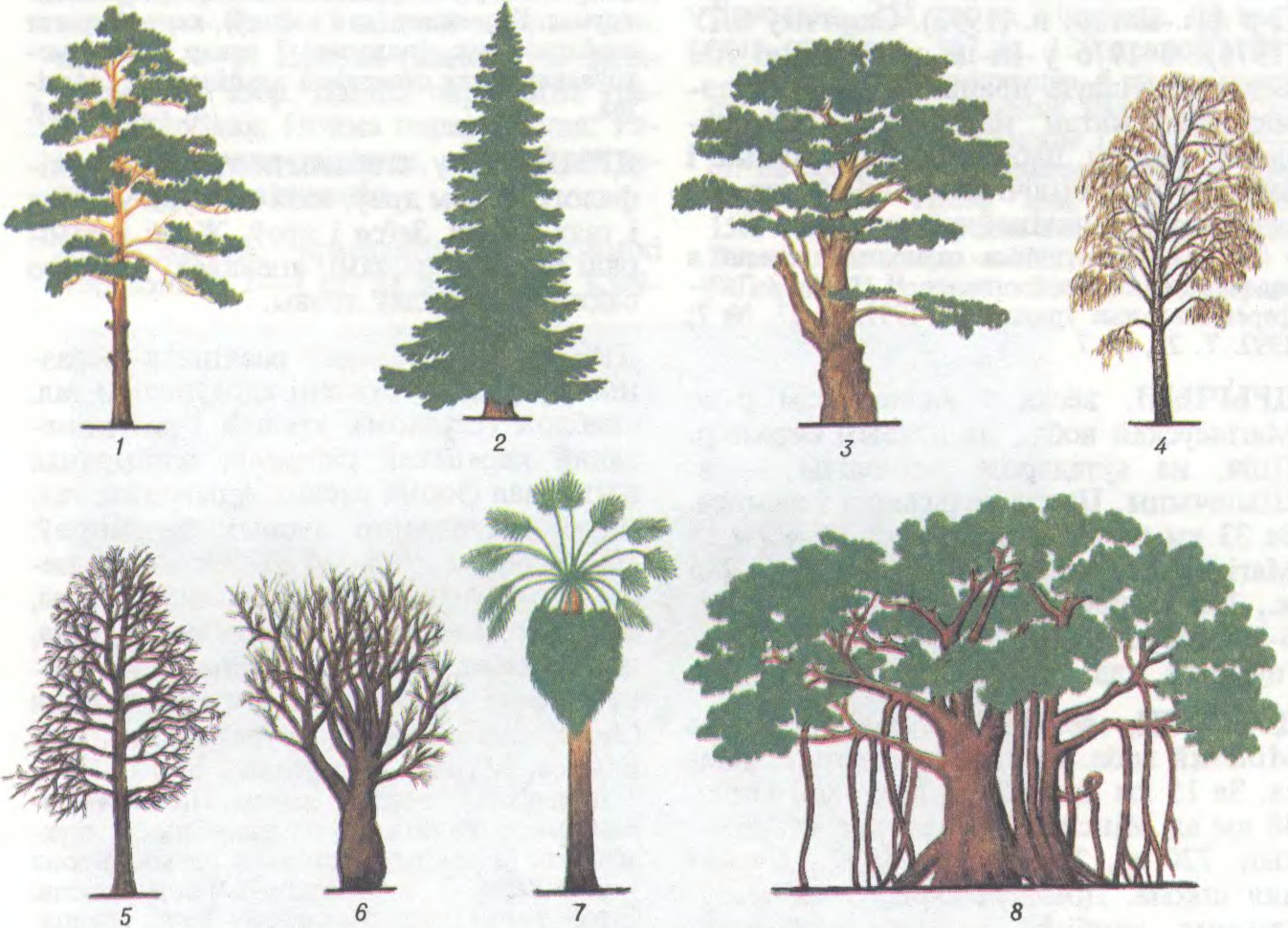
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ЖАЛЕ́ЗА ЗЛУЧЭ́ННІ,
хімічныя злучэнні, у састаў якіх уваходзіць жалеза, пераважна ў
І.В.Боднар.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
КАМУНІ́ЗМ (ад
агульная назва шэрагу розных канцэпцый аб ідэальнай грамадскай арганізацыі, а таксама гіпатэтычнага грамадскага і
Найбольш раннія
У марксісцкай канцэпцыі К. — грамадска-
Літ.:
Платон.
Джонсон Х. Христиане и коммунизм:
Маркс К. Крытыка Гоцкай праграмы.
Энгельс Ф. Принципы коммунизма // Маркс К., Энгельс Ф.
Ленин В.И. О социализме и коммунизме.
Зиновьев А.А. Коммунизм как реальность;
Кризис коммунизма.
Сорокин П.А. Человек. Цивилизация. Общество.
Данилов А.Н. Переходное общество: Пробл. системной трансформации.
Р.Ч.Лянькевіч.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
КРА́НАХ (Cranach) Лукас
(1472,
нямецкі жывапісец і графік эпохі Адраджэння. Вучыўся, магчыма, у бацькі. У 1505—50 працаваў пераважна ў Вітэнбергу пры двары курфюрстаў Саксонскіх. Рэнесансавыя
Літ.:
Немилов А.Н. Л.Кранах Старший: [Альбом].
В.Я.Буйвал.


Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ЛЕ́КСІКА (ад
сукупнасць усіх слоў пэўнай мовы, яе слоўнікавы склад і ўзровень. У больш вузкім значэнні
Літ.:
Гістарычная лексікалогія беларускай мовы.
Шмелев Д.Н. Современный русский язык: Лексика.
Методы изучения лексики.
Лексікалогія сучаснай беларускай літаратурнай мовы.
Беларускае слова ў тэксце і ў сістэме мовы.
В.К.Шчэрбін.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)