КА́ЛІЮ ЗЛУЧЭ́ННІ,
хімічныя злучэнні, у састаў якіх уваходзіць калій.
А.П.Чарнякова.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
КА́ЛІЮ ЗЛУЧЭ́ННІ,
хімічныя злучэнні, у састаў якіх уваходзіць калій.
А.П.Чарнякова.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МА́САВАЯ ЛІТАРАТУ́РА,
шматтыражная
Літ.:
«Массовая культура» — иллюзии и действительность.
Николюкин А.Н. Антикультура: массовая литература США
Шабловская И.В. Реализм и «массовая культура» // Шабловская И.В. История зарубежной литературы (XX в., первая половина).
І.В.Шаблоўская.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МЫ́ЛЫ,
солі вышэйшых (з 12—22 атамамі вугляроду ў малекуле) тлустых, а таксама нафтэнавых і смаляных кіслот; у вытв-сці і быце —
Малекулы М. складаюцца з непалярных (вуглевадародных) і палярных (іонагенных) частак. Пры пэўнай канцэнтрацыі раствору, якая
Ф.М.Капуцкі.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
НА́ТРЫЮ ЗЛУЧЭ́ННІ,
хімічныя злучэнні, у састаў якіх уваходзіць натрый. Для натрыю
Солі неарган. кіслот (пры бясколерным аніёне) — бясколерныя
А.П.Чарнякова.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
БЫТАВА́Я МУ́ЗЫКА,
музыка, якая функцыянуе ў штодзённым прыватным і грамадскім жыцці людзей, выконваецца па-за канцэртнай залай,
Вытокі бытавой музыкі ў глыбокай старажытнасці, калі музыка была неаддзельная ад
На Беларусі з 2-й
Літ.:
Асафьев Б.В. Русская музыка, XIX и начало XX века.
Яго ж. Бытовая музыка после Октября // Новая музыка.
Сохор А.Н. Эстетическая природа жанра в музыке // Сохор А.Н. Вопросы социологии и эстетики музыки.
Щербакова Т. Быт — бытовой диалект — классика // Сов. музыка. 1986. № 4;
Костюковец Л.Ф. Кантовая культура в Белоруссии.
Капилов А.Л. Скрипка белорусская.
Т.А.Шчарбакова.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ВЯРБА́ (Salix),
род кветкавых раслін
Лістападныя двухдомныя насякомаапыляльныя дрэвы, кусты і кусцікі. Лісце суцэльнае, чаргаванае, рэдка — супраціўнае. Кветкі аднаполыя, дробныя, без калякветніка, з нектарнікамі, у прамастойных ці павіслых мужчынскіх і жаночых каташках. Цвітуць ранняй вясной да распускання лісця. Плод — шматнасенная каробачка. Насенне з доўгаваласістай лятучкай.
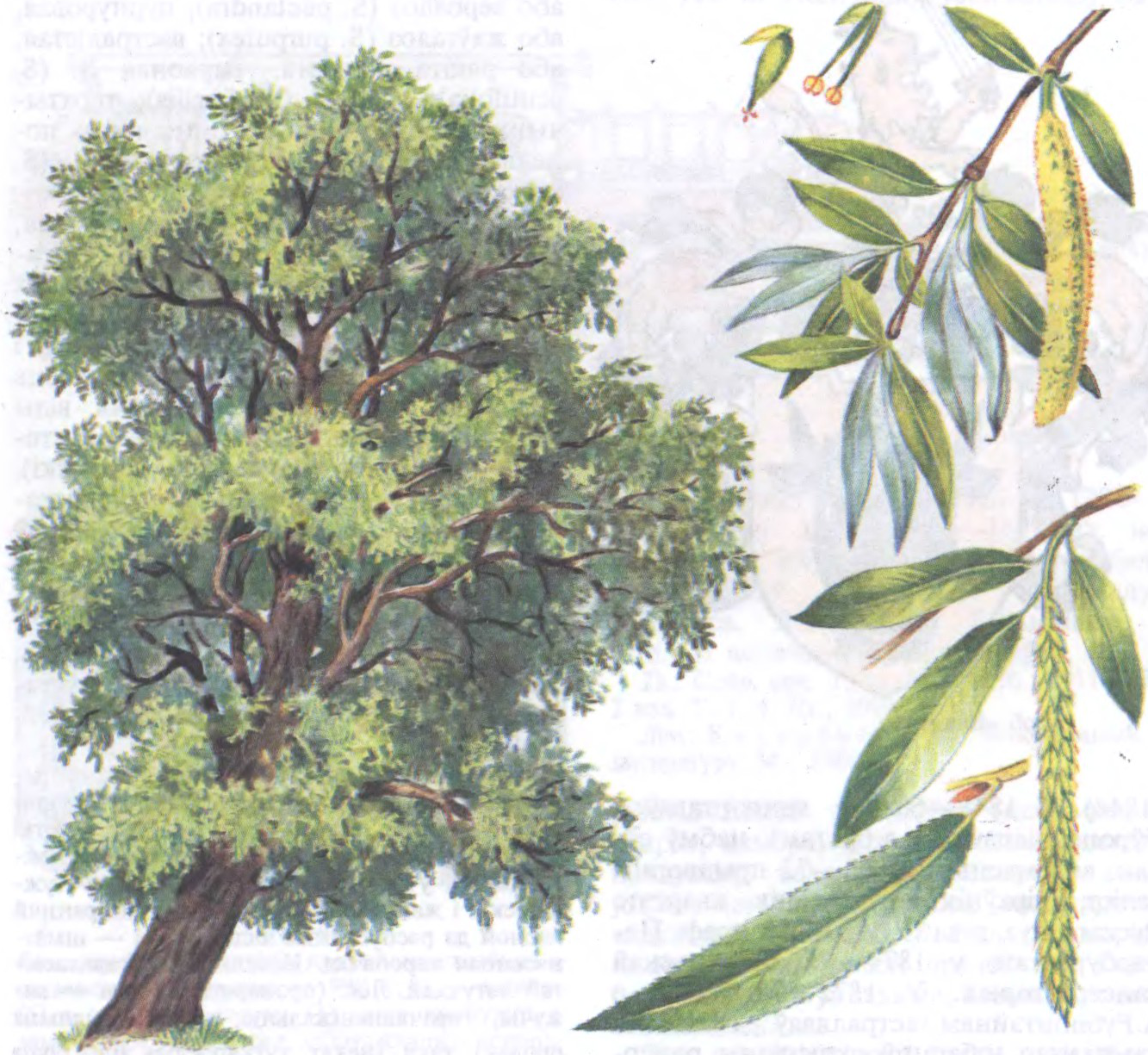
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
КА́ЛЬЦЫЮ ЗЛУЧЭ́ННІ,
хімічныя злучэнні, у састаў якіх уваходзіць кальцый.
А.П.Чарнякова.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МАЛЮ́СКІ (Mollusca),
Даўж. ад 1,1
Літ.:
Жизнь животных.
Фауна
Т.М.Лаенка.

Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
БЯРО́ЗА (Betula),
род кветкавых раслін
Аднадомныя лістападныя дрэвы або кусты і кусцікі з гладкай ці трэшчынаватай, часцей белай, радзей шэрай і
В.Ф.Пабірушка.


Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ЖАЛЕ́ЗА (
Fe, хімічны элемент VIII групы
Ж. — бліскучы серабрыста-белы пластычны метал tпл 1535
Літ.:
Беккерт М. Железо: Факты и легенды:
І.В.Боднар.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)