КАРБАНА́ТЫ,
солі і эфіры вугальнай кіслаты H2CO3.
К. 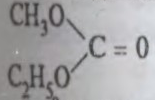 метылэтылкарбанат, tкіп 107
метылэтылкарбанат, tкіп 107
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
КАРБАНА́ТЫ,
солі і эфіры вугальнай кіслаты H2CO3.
К. 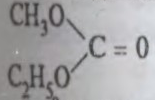 метылэтылкарбанат, tкіп 107
метылэтылкарбанат, tкіп 107
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ДУБІ́ЛЬНЫЯ РЭ́ЧЫВЫ,
рэчывы, якія выкарыстоўваюць для дублення скуры і футра. Паводле
Мінеральныя Д.р. — солі хрому, алюмінію, цырконію, жалеза, тытану і
Я.Г.Міляшкевіч.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
БІЯЛАГІ́ЧНЫЯ МЕМБРА́НЫ,
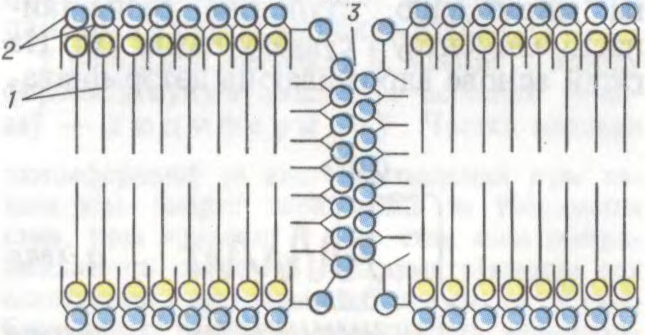
тонкія пагранічныя паўпранікальныя бялкова-ліпідныя малекулярныя структуры на паверхні клетак і субклетачных часціц (арганел), а таксама канальцаў і пузыркоў, што пранізваюць пратаплазму. Таўшчыня не больш за 10 нм. Складзены з бімалекулярнага слоя ліпідаў (пераважна фосфаліпідаў), у якім размешчаны розныя мембранныя бялкі, гетэрагенныя макрамалекулы (глікапратэіды, глікаліпіды) і розныя мінорныя кампаненты (нуклеінавыя к-ты, каферменты, караціноіды і
А.М.Ведзянееў.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МА́ГНІЙ (
Mg, хімічны элемент II групы
І.В.Боднар.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
БІЯЭЛЕКТРЫ́ЧНЫЯ ПАТЭНЦЫЯ́ЛЫ,
электрычныя патэнцыялы, якія ўзнікаюць у жывых тканках і асобных клетках чалавека, жывёл і раслін; паказчык біяэл. актыўнасці; важнейшыя кампаненты працэсаў узбуджэння і тармажэння. Вызначаюцца іх рознасцю паміж двума пунктамі жывой тканкі.
А.М.Ведзянееў, У.У.Салтанаў.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ГОРНАХІМІ́ЧНАЯ ПРАМЫСЛО́ВАСЦЬ,
галіна горназдабыўной прамысловасці, якая займаецца здабычай, першаснай перапрацоўкай і абагачэннем сыравіны (фасфатных, серных, борных, мыш’яковых, барыевых і барытавых руд, прыродных сульфату
Узнікненне горнахімічнай прамысловасці як
У Беларусі развіццё горнахімічнай прамысловасці пачалося з адкрыцця ў 1949 Старобінскага радовішча калійных і каменнай солей (буйнейшае ў свеце). На базе іх здабычы і перапрацоўкі ўзнік
А.А.Саламонаў.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МЫ́ЛЫ,
солі вышэйшых (з 12—22 атамамі вугляроду ў малекуле) тлустых, а таксама нафтэнавых і смаляных кіслот; у вытв-сці і быце —
Малекулы М. складаюцца з непалярных (вуглевадародных) і палярных (іонагенных) частак. Пры пэўнай канцэнтрацыі раствору, якая
Ф.М.Капуцкі.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
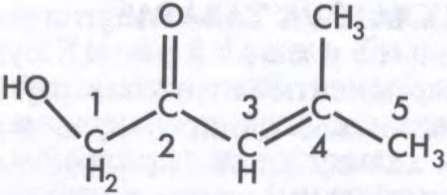
НАМЕНКЛАТУ́РА ХІМІ́ЧНАЯ,
сістэма назваў
Да канца 18
Літ.:
Номенклатурные правила ИЮПАК по химии:
Кан Р., Дермер О. Введение в химическую номенклатуру:
Бокий Г.Б., Голубкова Н.А. Введение в номенклатуру ИЮПАК
Міляшкевіч Я.Г. Этапы станаўлення беларускай хімічнай тэрміналогіі // Хімія: Прабл. выкладання. 1996.
Т.Т.Лахвіч.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ГІДРО́ЛІЗ (ад гідра... + ...ліз),
рэакцыя абменнага ўзаемадзеяння паміж рэчывам і вадой.
Пры гідролізе солей, утвораных слабай асновай і моцнай к-той (
Т.П.Цэдрык.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МЁРТВАЕ МО́РА,
бяссцёкавае салёнае возера на мяжы Ізраіля і Іарданіі. Займае самую нізкую
А.М.Матузка.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)