МАЛІБДА́ТЫ,
солі малібдэнавых кіслот.
Монамалібдаты, ці нармальныя
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МАЛІБДА́ТЫ,
солі малібдэнавых кіслот.
Монамалібдаты, ці нармальныя
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
сты́ракс
(
1) дрэвавая або кустовая расліна
2) пахучы бальзам, які атрымліваюць з гэтай расліны і выкарыстоўваюць у парфумерыі і медыцыне.
Слоўнік іншамоўных слоў (А. Булыка, 1999, правапіс да 2008 г.)
сума́х
(
дрэвавая або кустовая расліна
Слоўнік іншамоўных слоў (А. Булыка, 1999, правапіс да 2008 г.)
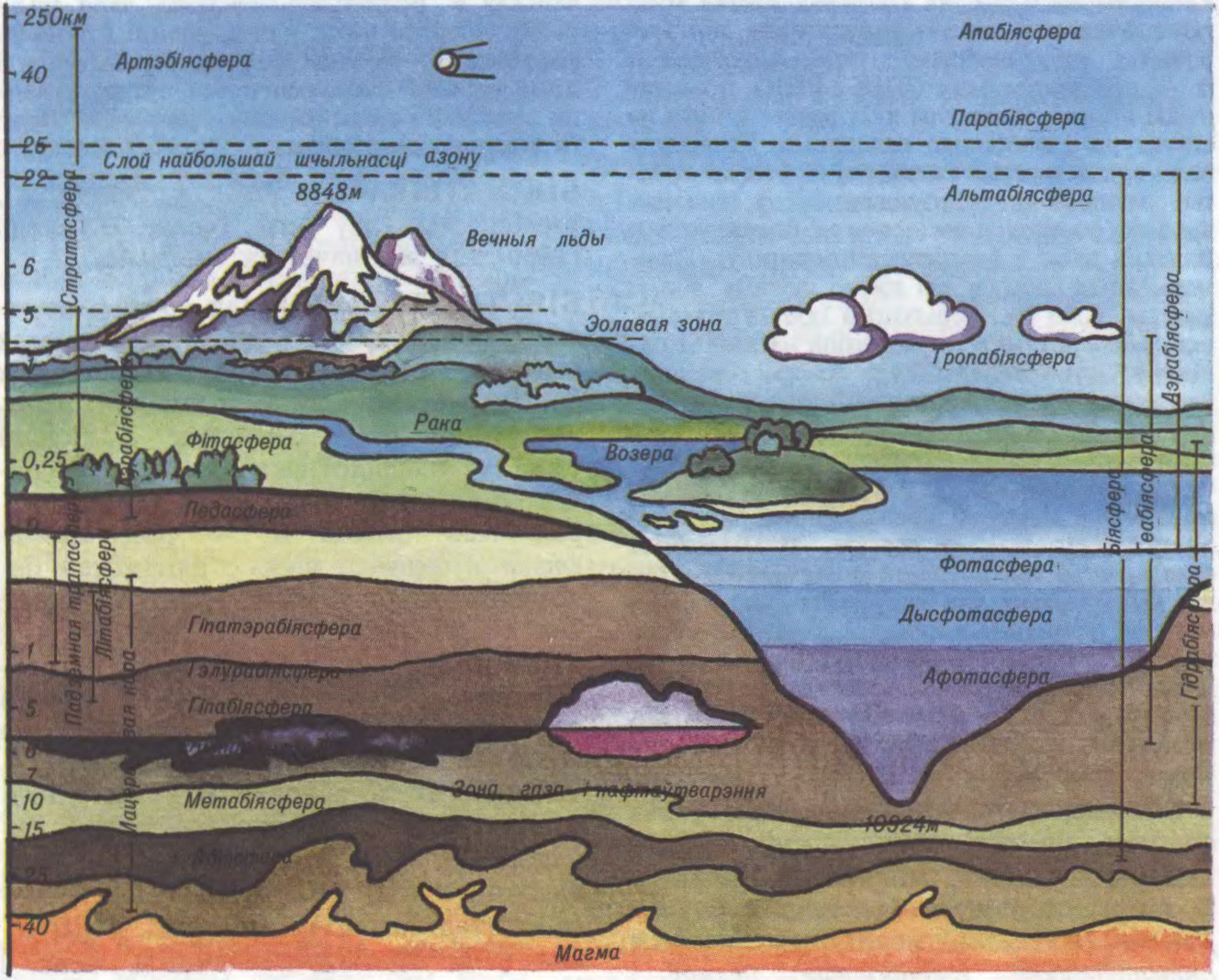
БІЯСФЕ́РА (ад бія... + сфера),
абалонка Зямлі, састаў, структура і энергетыка якой абумоўлены сукупнай дзейнасцю і ўплывамі жывых арганізмаў. Першыя ўяўленні пра біясферу сфармуляваў
Літ.:
Вернадский В.И. Химическое строение биосферы Земли и ее окружения. 2 изд.
Никитин Д.П., Новиков Ю.В. Окружающая среда и человек 2 изд.
Сытник К.М., Брайон А.В., Гордецкий А.В. Биосфера, экология, охрана природы: Справ. пособие. Киев, 1987.
Г.А.Семянюк.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ко́рань, -я,
1. Падземная частка расліны, пры дапамозе якой яна замацоўваецца ў зямлі і атрымлівае пажыўныя
2. Частка зуба, ногця, воласа
3.
4. У граматыцы: асноўная частка слова без суфікса і прыстаўкі.
5. У матэматыцы: лік, які пры ўзвядзенні ў пэўную ступень дае дадзены лік.
Глядзець у корань (
Вырваць з коранем — канчаткова пазбавіцца ад чаго
На корані — пра расліны: не зжаты, не скошаны.
Пад корань —
1) ля самай асновы (ссякаць, зразаць што
2) канчаткова (разбураць, знішчаць).
Пусціць карані — трывала, надоўга абаснавацца дзе
У корані —
1) зусім, абсалютна (не згаджацца з чым
2) у самай аснове, карэнным чынам (змяняць
||
||
Тлумачальны слоўнік беларускай літаратурнай мовы (І. Л. Капылоў, 2022, актуальны правапіс)
кана́л, ‑а,
1. Напоўненае вадой штучнае рэчышча, прызначанае для суднаходнай сувязі паміж асобнымі вадаёмамі, а таксама для водазабеспячэння, арашэння, асушэння балот і інш.
2. Вузкая поласць у выглядзе трубы, трубкі ўнутры чаго‑н.
3. У арганізме жывёлы і чалавека — звілістая трубка, праз якую праходзяць тыя ці іншыя
4.
5.
[Ад лац. canalis — труба.]
Тлумачальны слоўнік беларускай мовы (1977-84, правапіс да 2008 г.)
ГАЛЫ́Н,
комплексныя злучэнні, крышталегідраты двайных сульфатаў саставу M1MIII(SO4)2∙12H2O ці MI2SO4 × M2III(SO4)3∙24H2O (MI — адназарадны катыён: Na+, K+, Rb+, Cs+, NH4+ і
Вядома некалькі дзесяткаў галынаў. Пры звычайных умовах устойлівыя
У прыродзе трапляецца алюмакаліевы, алюманатрыевы (мінерал чэрмігіт). Выкарыстоўваюць у
І.В.Боднар.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ГАРМАНА́ЛЬНЫЯ ПРЭПАРА́ТЫ,
Гарманальныя прэпараты гіпаталамуса і гіпофіза — кортыкатрапін, які стымулюе дзейнасць кары наднырачнікаў, самататрапін — рост арганізма, тыратрапін — сакрэцыю гармонаў шчытападобнай залозы, саматастацін прыгнечвае выпрацоўку гармону росту, лактын павялічвае выдзяленне малака малочнымі залозамі пасля родаў, ганадатрапін стымулюе функцыю палавых залоз, аксітацын, пітуітрын — мускулатуру маткі, вазапрэсін — гладкую мускулатуру. Гарманальныя прэпараты шчытападобнай і парашчытападобнай залозы (тырэаідзін, тыратаксін, паратырэаідзін) назначаюць пры недастатковай функцыі гэтых залоз; кальцытацын рэгулюе абмен кальцыю. Гарманальныя прэпараты падстраўнікавай залозы — інсулін ужываюць пры
А.С.Захарэўскі.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ВА́ДКАСЦЬ,
агрэгатны стан рэчыва, прамежкавы паміж цвёрдым і газападобным.
Цеплавы рух малекул вадкасці складаецца з ваганняў каля стану раўнавагі і рэдкіх пераскокаў з аднаго раўнаважнага стану ў іншы, чым абумоўлена
Літ.:
Крокстон К. Физика жидкого состояния:
Динамические свойства твердых тел и жидкостей:
В.І.Навуменка.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ГЕРМА́НІЙ (
Ge, хімічны элемент IV групы перыядычнай сістэмы,
Цвёрдае крохкае рэчыва серабрыстага колеру з
І.В.Боднар.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)