МЕТЭАРАЛАГІ́ЧНЫЯ ПРЫЛА́ДЫ,
прылады, якія служаць для рэгістрацыі і вымярэння разнастайных метэаралагічных элементаў. Існуюць М.п. з візуальным адлікам і з
Г.Г.Камлюк.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МЕТЭАРАЛАГІ́ЧНЫЯ ПРЫЛА́ДЫ,
прылады, якія служаць для рэгістрацыі і вымярэння разнастайных метэаралагічных элементаў. Існуюць М.п. з візуальным адлікам і з
Г.Г.Камлюк.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ПАДЗЕ́МНЫЯ ВО́ДЫ,
воды ў тоўшчы горных парод верхняй часткі
На
Літ.:
Государственный водный кадастр: Водные ресурсы, их использование и качество вод (за 1996
Альтшуль А.Х., Усенко В.С., Чабан М.О. Регулирование запасов подземных вод.
Кудельский А.В., Пашкевич В.И., Ясовеев М.Г. Подземные воды Беларуси.
Калинин М.Ю. Подземные воды и устойчивое развитие.
В.С.Усенка.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
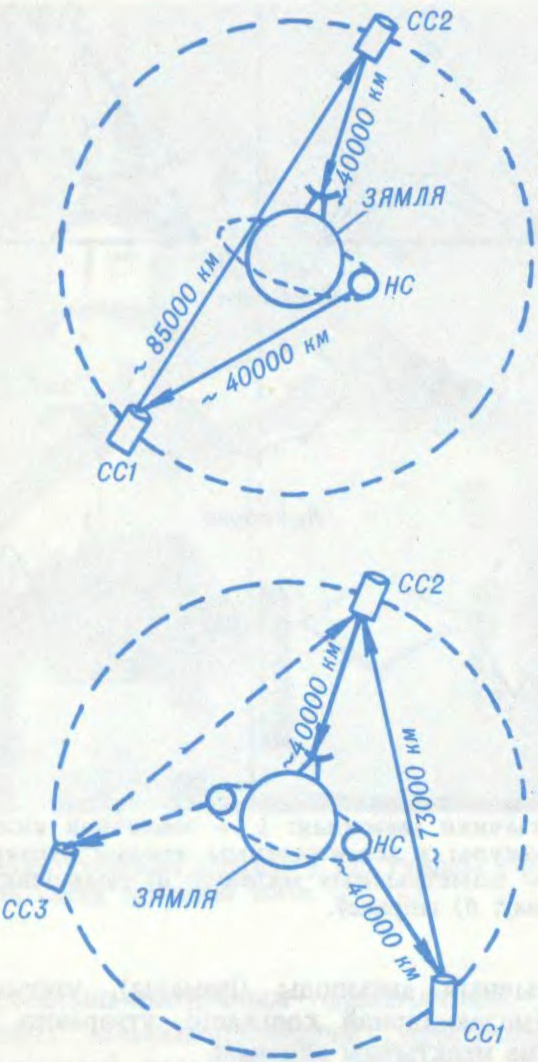
АПТЫ́ЧНАЯ СУ́ВЯЗЬ,
перадача інфармацыі з дапамогай
Для мадуляцыі лазернага выпрамянення ўздзейнічаюць на працэс яго генерацыі або выкарыстоўваюць мадулятар святла. На выхадзе перадатчыка фарміруецца вузкі маларазбежны прамень святла; трапляючы на ўваход прыёмніка, ён накіроўваецца на фотадэтэктар, дзе аптычнае выпрамяненне пераўтвараецца ў
Літ.:
Алишев Я.В. Многоканальные системы передачи оптического диапазона.
Волоконно-оптические системы передачи.
Я.В.Алішаў.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
БІЯГЕАХІ́МІЯ (ад бія... + геахімія),
галіна геахіміі, якая вывучае
Заснавальнік біягеахіміі —
І.К.Вадкоўская.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
БІЯЛАГІ́ЧНЫ КРУГАВАРО́Т,
паступленне
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ГАЗ (
агрэгатны стан рэчыва, у якім слаба звязаныя малекулярнымі сіламі часціцы рухаюцца свабодна і пры адсутнасці знешніх палёў раўнамерна запаўняюць увесь дадзены ім аб’ём. Газ, у якім энергію ўзаемадзеяння паміж часціцамі можна не ўлічваць,
Рэальныя газы пры звычайных умовах мала адрозніваюцца ад ідэальнага, а пры памяншэнні ціску і павышэнні т-ры па ўласцівасцях набліжаюцца да яго; часцей іх стан апісваецца Ван-дэр-Ваальса ўраўненнем. Пры паніжэнні т-ры газы дасягаюць крытычнага стану, пры далейшым ахаладжэнні і павышэнні ціску адбываецца звадкаванне газаў. Калі рух часціц падпарадкоўваецца законам класічнай механікі, газ
А.І.Болсун.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ЗО́ЛАТА (Aurum),
Au, хімічны элемент I групы
Жоўты мяккі і вельмі пластычны метал,
Літ.:
Баукова Т.В., Леменовский Д.А. Золото в химии и медицине.
І.В.Боднар.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ЛАНДША́ФТ ГЕАГРАФІ́ЧНЫ,
адносна аднародны ўчастак
Літ.:
Ландшафты Белоруссии.
В.С.Аношка.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ЛІ́ТЫЙ (
Li, хімічны элемент I
Мяккі і пластычны серабрыста-беды метал,
І.В.Боднар.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МА́ГНІЙ (
Mg, хімічны элемент II групы
І.В.Боднар.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)