КА́ЛІЮ ЗЛУЧЭ́ННІ,
хімічныя злучэнні, у састаў якіх уваходзіць калій.
А.П.Чарнякова.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
КА́ЛІЮ ЗЛУЧЭ́ННІ,
хімічныя злучэнні, у састаў якіх уваходзіць калій.
А.П.Чарнякова.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
НА́ТРЫЮ ЗЛУЧЭ́ННІ,
хімічныя злучэнні, у састаў якіх уваходзіць натрый. Для натрыю
Солі неарган. кіслот (пры бясколерным аніёне) — бясколерныя
А.П.Чарнякова.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
КА́ЛЬЦЫЮ ЗЛУЧЭ́ННІ,
хімічныя злучэнні, у састаў якіх уваходзіць кальцый.
А.П.Чарнякова.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
КАРМАВЫ́Х БЯЛКО́ВЫХ РЭ́ЧЫВАЎ ПРАМЫСЛО́ВАСЦЬ,
галіна мікрабіялагічнай прамысловасці. Вырабляе бялковыя кармавыя рэчывы, пераважна кармавыя дрожджы, з вуглевадароднай і расліннай сыравіны для жывёлагадоўлі. Уключае таксама прадпрыемствы гідролізнай прамысловасці і
Прадпрыемствы, якія выкарыстоўваюць вуглевадародную сыравіну з-за высокай матэрыялаёмістасці прадукцыі найчасцей арыентуюцца на цэнтры нафтаперапрацоўкі. Для атрымання 1
На Беларусі вытворчасць карм. бялковых рэчываў развіваецца з канца 1960-х
Г.С.Смалякоў.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ЛЕ́КАВЫЯ СРО́ДКІ,
рэчывы, якія выкарыстоўваюць у мэтах дыягностыкі, прафілактыкі і лячэння захворванняў чалавека і жывёл. У якасці Л.с. выкарыстоўваюць
Літ.:
Машковский М.Д. Лекарственные средства: Пособие для врачей.
Базисная и клиническая фармакология:
Регистр лекарственных средств Росии: Энцикл. лекарств.
М.К.Кеўра.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МЕ́ДЗІ ЗЛУЧЭ́ННІ,
хімічныя злучэнні, у састаў якіх уваходзіць медзь.
А.П.Чарнякова.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
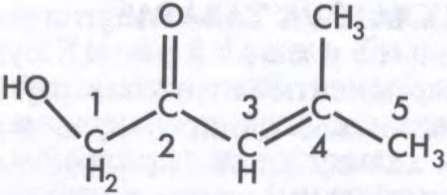
НАМЕНКЛАТУ́РА ХІМІ́ЧНАЯ,
сістэма назваў
Да канца 18
Літ.:
Номенклатурные правила ИЮПАК по химии:
Кан Р., Дермер О. Введение в химическую номенклатуру:
Бокий Г.Б., Голубкова Н.А. Введение в номенклатуру ИЮПАК
Міляшкевіч Я.Г. Этапы станаўлення беларускай хімічнай тэрміналогіі // Хімія: Прабл. выкладання. 1996.
Т.Т.Лахвіч.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)