КРЭ́МНІЙ (
Si, хімічны элемент IV групы
Крышт. К. — цёмна-шэрае рэчыва з
А.П.Чарнякова.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
КРЭ́МНІЙ (
Si, хімічны элемент IV групы
Крышт. К. — цёмна-шэрае рэчыва з
А.П.Чарнякова.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МА́РГАНЕЦ (
Серабрыста-белы метал, tпл 1244
А.П.Чарнякова.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
gaz, ~u
Польска-беларускі слоўнік (Я. Волкава, В. Авілава, 2004, правапіс да 2008 г.)
ГАРАДСКА́Я ГАСПАДА́РКА,
комплекс службаў, прадпрыемстваў, арг-цый,
Літ.:
Проектирование городского хозяйства. 3 изд.
Чекалин В.С., Томилов В.В. Перспективное планирование капитального ремонта объектов городского хозяйства.
Хатунцев В.М., Валахова В.Д. Основы финансово-кредитной системы городского хозяйства.
.М.Удавенка.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ВЯЗЬ,
старажытнае 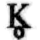 ; памяншэнне памеру абедзвюх літар і напісанне іх адна пад адной (МР =
; памяншэнне памеру абедзвюх літар і напісанне іх адна пад адной (МР = 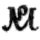 ); зліццё падобных частак суседніх літар (ПР =
); зліццё падобных частак суседніх літар (ПР = 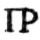 ). Упрыгожванне служыла для запаўнення пустот, уласцівых многім
). Упрыгожванне служыла для запаўнення пустот, уласцівых многім
Першапачаткова вязь выкарыстоўвалася ў загалоўках і надпісаннях. На Русі з’явілася ў 14
М.А.Паўленка, А.М.Булыка.

Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ВАДАРО́Д,
H, хімічны элемент VII групы
Малекула вадароду двухатамная. Пры звычайных умовах узаемадзейнічае толькі з фторам і хлорам (на святле), пры павышаных т-рах у прысутнасці каталізатараў — з кіслародам (
Газападобны вадарод выкарыстоўваюць для сінтэзу аміяку, хлорыстага вадароду, метылавага і вышэйшых спіртоў, вуглевадародаў, для гідрагенізацыі тлушчу, таксама для зваркі і рэзкі металаў вадародна-кіслародным полымем, вадкі — як гаручае ў ракетнай і
І.В.Боднар.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ГЕ́ЛІЙ (
Не, хімічны элемент VII групы перыядычнай сістэмы,
Аднаатамны газ без колеру і паху, tкіп -268,39
В.Р.Собаль.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
КІСЛАРО́Д (
O, хімічны элемент VI групы
К. — газ без колеру і паху,
Літ.:
Глизманенко Д.Л. Получение кислорода. 5 изд.
Разумовский С.Д. Кислород — элементарные формы и свойства.
В.В.Свірыдаў.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МІНЕРА́ЛЬНЫЯ РЭСУ́РСЫ,
сукупнасць карысных выкапняў, выяўленых у нетрах асобных рэгіёнаў, краін, кантынентаў, прыдатных і даступных для асваення. З’яўляюцца сыравіннай асновай для развіцця найважнейшых галін
Частка М.р., падрыхтаваная геолагаразведачнымі работамі да асваення,
П.З.Хоміч.
| Карысныя выкапні | Еўропа (без Расіі) | Азія (без Расіі) | Расія | Афрыка | Амерыка | Акіянія і Аўстралія | Усяго сусветных запасаў |
| Нафта, уключна з газавым кандэнсатам, млн.т | 2964,5 | 97220,7 | 21252,9 | 10252,3 | 22822,4 | 560,6 | 155073,4 |
| 6425,4 | 61108,8 | 47380 | 9302,2 | 14571 | 618,3 | 139405,7 | |
| Вугаль, млн.т | 676002 | 1323605 | 279582 | 178138 | 1894884 | 879700 | 5231911 |
| Уран, тыс.т | 969,84 | 5675,44 | 1586 | 2079,77 | 5606,66 | 895 | 16812,71 |
| Жалезная руда, млн.т | 52042 | 54309 | 100909 | 52499 | 88056 | 33440 | 381255 |
| Марганцавая руда, млн.т | 2560 | 1383 | 152 | 5139 | 889 | 267 | 10390 |
| Хромавыя руды, млн.т | 132,7 | 1322,4 | 310,28 | 13051,5 | 553 | 127 | 15496,88 |
| Баксіты, млн.т | 2098 | 8284 | 674 | 26459 | 14802 | 9903 | 62220 |
| Вальфрамавыя руды (у пераліку на аксід), тыс.т | 350 | 2332 | 420 | 62 | 903 | 34 | 4101 |
| Медныя руды (у пераліку на метал), тыс.т | 80002 | 226699 | няма звестак | 83348 | 509028 | 33509 | 932586 |
| Малібдэнавыя руды (у пераліку на метал), тыс.т | 10 | 3861 | няма звестак | 19 | 9706 | 109 | 13705 |
| Нікелевыя руды (у пераліку на метал), тыс.т | 8420 | 28400 | 7300 | 17730 | 39295 | 31010 | 132155 |
| Алавяныя руды (у пераліку на метал), тыс.т | 285 | 4850 | 300 | 680 | 3555 | 400 | 10070 |
| Свінцовыя руды ( у пераліку на метал), тыс.т | 28983 | 79307 | 14150 | 16850 | 55675 | 24400 | 219365 |
| Цынкавыя руды (у пераліку на метал), тыс.т | 66636 | 182790 | няма звестак | 35470 | 139650 | 65000 | 489546 |
| Калійныя солі (у пераліку на аксід), млн.т | 3296 | 2780 | 19118 | 179 | 14915 | няма звестак | 40288 |
| Фасфатныя руды (апатыты і фасфарыты), млн.т | 1647,1 | 17996,1 | 4827,5 | 20715,3 | 23509,5 | 927,6 | 69623,1 |
| Серабро, т | 156700 | 194100 | няма звестак | 53600 | 339000 | 55400 | 798800 |
| Золата, т | 2532 | 14212 | няма звестак | 43328 | 24913 | 6365 | 91350 |
| Алмазы, млн. каратаў | няма звестак | 52 | няма звестак | 3243,1 | 817 | 705 | 4817,1 |
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
Роў 1 ’доўгае паглыбленне ў зямлі, канава’ (
Роў 2 ’моцны працяглы крык некаторых жывёл’, ’гукі, што напамінаюць такі крык’, ’моцны плач’ (
Этымалагічны слоўнік беларускай мовы (1978-2017)