КАТАБАЛІ́ЗМ (ад
Літ.:
Я.В.Малашэвіч.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
КАТАБАЛІ́ЗМ (ад
Літ.:
Я.В.Малашэвіч.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
КРЫШТАЛЯХІ́МІЯ,
раздзел хіміі, у якім вывучаюцца прасторавае размяшчэнне і характар узаемадзеяння паміж атамамі, іонамі, малекуламі, з якіх складаюцца крышталі, а таксама сувязь паміж структурай крышталёў і іх уласцівасцямі.
Асн. характарыстыкай структуры крышталёў з’яўляецца элементарная ячэйка, якая адлюстроўвае характар сіметрыі крышталёў, узаемнае размяшчэнне, каардынацыйны лік і адлегласці паміж атамамі (іонамі, малекуламі) у крышталях. Элементарныя ячэйкі маюць форму шматграннікаў, а сукупнасць такіх шматграннікаў з агульнымі гранямі складае прасторавую крышталічную рашотку. К. вызначае фактары, якімі абумоўлены характар сіметрыі і структура элементарнай ячэйкі; устанаўлівае тып крышталёў — іх прыналежнасць да кавалентных (атамы ў рашотцы злучаны кавалентнай сувяззю), іонных крышталёў,
Літ.:
Бокий Г.Б. Кристаллохимия. 3 изд.
Урусов В.С. Теоретическая кристаллохимия.
Уэллс А.Ф. Структурная неорганическая химия:
В.В.Свірыдаў.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МАЛЕКУЛЯ́РНАЯ МА́СА,
маса малекулы, выражаная ў атамных адзінках масы; адна з канстантаў, якая характарызуе індывідуальнае рэчыва. М.м. роўная суме мас атамаў, што ўваходзяць у склад малекулы. М.м. (абазначаецца М або μ) уваходзіць у многія ўраўненні і суадносіны, якімі карыстаюцца пры разліках у хіміі і фізіцы. У хіміі і
Асн. метадам вызначэння М.м. лятучых рэчываў з’яўляецца мас-спектраметрыя. Вызначэнне М.м. нелятучых і недысацыіруючых у растворах рэчываў заснавана на вымярэнні калігатыўных уласцівасцей (г. зн. уласцівасцей, якія залежаць ад колькасці раствораных часціц) — паніжэння ціску пары (апісваецца законам Рауля) і т-ры замярзання (
М.Р.Пракапчук.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
НІ́КЕЛЬ (
Ni, хімічны элемент VIII групы
Серабрыста-белы коўкі метал, tпл 1455
У.С.Камароў.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ПАДЗЕ́МНЫЯ ЗБУДАВА́ННІ,
спецыяльна абсталяваныя збудаванні, размешчаныя ў тоўшчы зямлі. Да іх адносяцца:
П.з. неглыбокага залажэння будуюць адкрытым спосабам (у катлаванах, траншэях), метадамі апускнога калодзежа або «сцяна ў грунце» (у траншэях робяцца сцены з наступным выманнем грунту з
На Беларусі П.з. з’яўляюцца Мінскі метрапалітэн, газасховішчы, аб’екты
І.І.Леановіч.

Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ЗАБРУ́ДЖВАННЕ ВОД,
працэс змены складу і ўласцівасцей вады, абумоўлены паступленнем у водныя аб’екты забруджвальнікаў, якія робяць воды непрыдатнымі для водакарыстання, пагаршаюць умовы пражывання жывых арганізмаў. Адрозніваюць прыроднае (натуральнае) З.в. і забруджванне антрапагеннае. Прыроднае З.в. выклікаецца паводкамі, размывам берагоў, забруджанымі
На Беларусі ў рэкі скідваецца некалькі кубічных кіламетраў сцёкаў за год (
Я.В.Малашэвіч.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
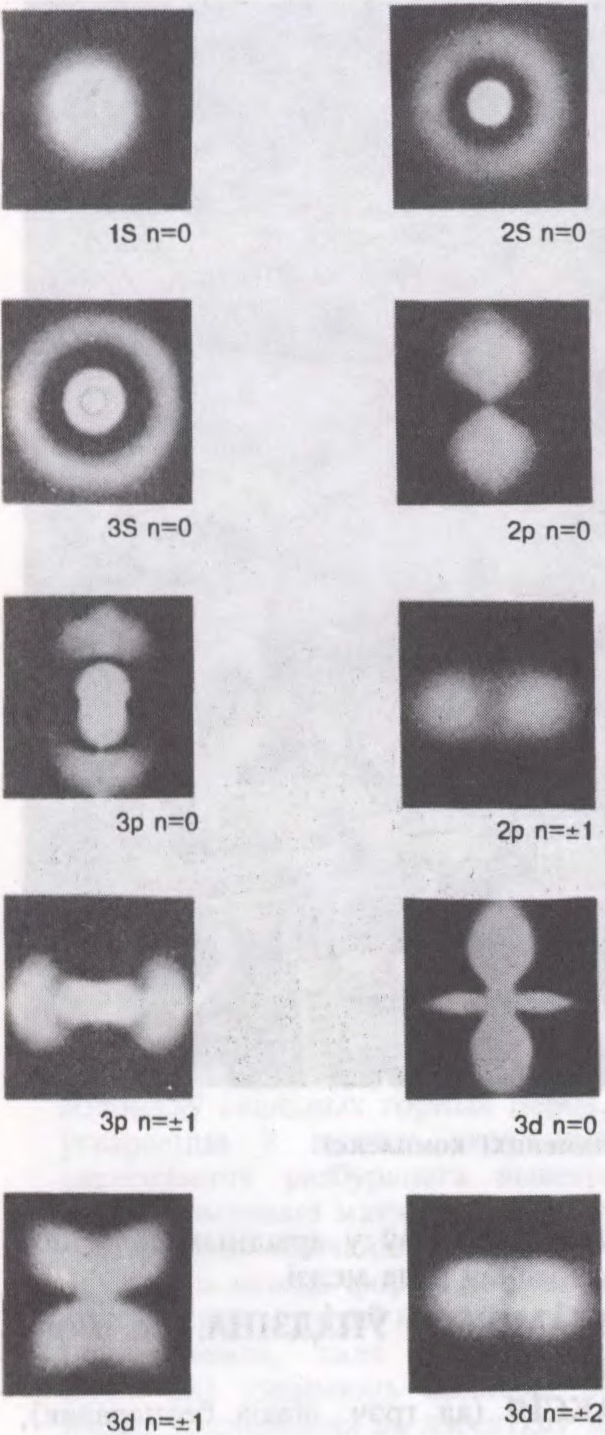
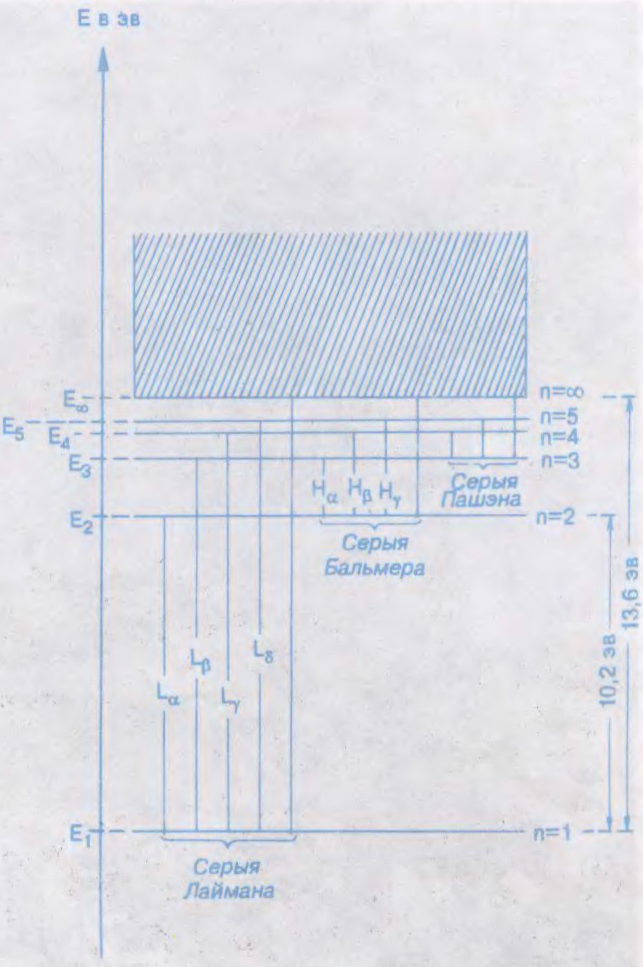
А́ТАМ (ад
часціца рэчыва, найменшая частка
Літ.:
Шпольский Э.В. Атомная физика. Т. 1—2.
Борн М. Атомная физика.
Гольдин Л.Л., Новикова Г.И. Введение в квантовую физику.
Ландау Л.Д., Лифшиц Е.М. Теоретическая физика. Т. 3. Квантовая механика;
Нерелятивистская теория. 4 изд.
М.А.Ельяшэвіч.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
АНТРАХІНО́НАВЫЯ ФАРБАВА́ЛЬНІКІ,
клас арганічных фарбавальнікаў, вытворных антрахінону. Адметныя
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
АНТЫВІТАМІ́НЫ (ад анты... + вітаміны),
рэчывы з ліку антыметабалітаў, якім уласціва
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
АНТЫСЕ́ПТЫКА (ад анты... +
комплекс лячэбна-прафілактычных мерапрыемстваў, накіраваных на знішчэнне патагенных мікробаў у пашкоджаных тканках або арганізме ў цэлым, на папярэджанне або ліквідацыю
У практыцы выкарыстоўваюць
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)