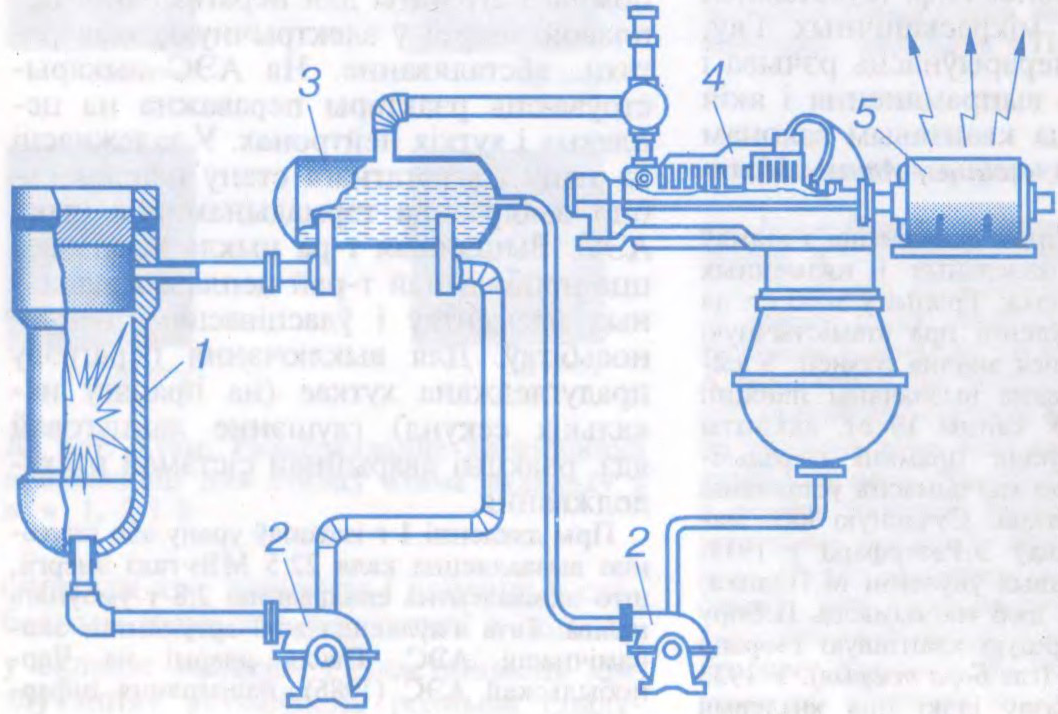
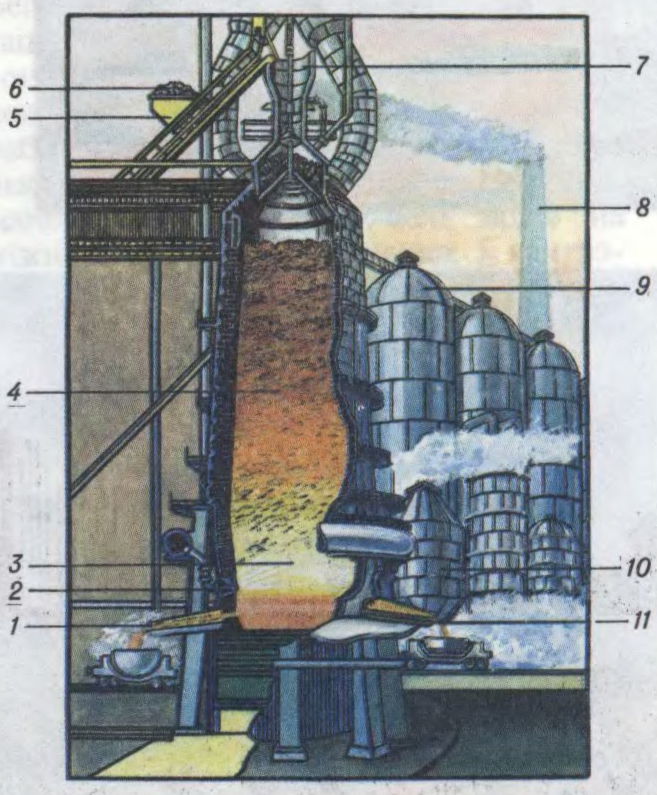
ВАДАРО́Д, гідраген (лац. Hydrogenium),
H, хімічны элемент VII групы перыяд. сістэмы, ат. н. 1, ат. м. 1,00794. Прыродны вадарод складаецца з 2 ізатопаў 1H (протый, 99,98% па масе) і 2H ці Д (дэйтэрый, 0,02%), атрыманы штучныя радыеактыўныя 3H ці T (трытый) і вельмі няўстойлівы 4H. У паветры колькасць вадароду 3,5∙10−6% па масе, у літасферы і гідрасферы — 1%, у вадзе — 11,19%, у складзе арганічных злучэнняў вадароду маюць усе раслінныя і жывёльныя арганізмы. Самы пашыраны элемент у космасе, складае каля палавіны масы Сонца, большасці зорак. Газ без колеру і паху, tпл -259,1 °C, tкіп -252,6 °C, шчыльн. вадкага 70,8 кг/м³ (-235 °C). Вадарод і яго сумесі з паветрам і кіслародам (гл. Грымучы газ) пажара- і выбухованебяспечныя.
Малекула вадароду двухатамная. Пры звычайных умовах узаемадзейнічае толькі з фторам і хлорам (на святле), пры павышаных т-рах у прысутнасці каталізатараў — з кіслародам (гл. Вада), галагенамі (гл. Галагенавадароды), азотам (гл. Аміяк). Са шчолачнымі і шчолачназямельнымі металамі, элементамі III—IV груп перыяд. сістэмы ўтварае гідрыды. Аднаўляе аксіды і галагеніды металаў да металаў, ненасычаныя вуглевадароды (гл. Гідрагенізацыя). Лёгка аддае электрон, у водных растворах пратон H+ існуе ў выглядзе іона гідраксонію, утварае вадародную сувязь. У прам-сці атрымліваюць канверсіяй метану: CH4 + 2H2O = 4H2 + CO2; пры газіфікацыі вадкага і цвёрдага паліва (гл. Вадзяны газ).
Газападобны вадарод выкарыстоўваюць для сінтэзу аміяку, хлорыстага вадароду, метылавага і вышэйшых спіртоў, вуглевадародаў, для гідрагенізацыі тлушчу, таксама для зваркі і рэзкі металаў вадародна-кіслародным полымем, вадкі — як гаручае ў ракетнай і касм. тэхніцы, ізатопы — у атамнай энергетыцы.
І.В.Боднар.
т. 3, с. 434