вале́нтнасць, ‑і,
[Ад лац. valens, valentis — які мае сілу.]
Тлумачальны слоўнік беларускай мовы (1977-84, правапіс да 2008 г.)
вале́нтнасць, ‑і,
[Ад лац. valens, valentis — які мае сілу.]
Тлумачальны слоўнік беларускай мовы (1977-84, правапіс да 2008 г.)
а́там, ‑а,
Найдрабнейшая часцінка хімічнага элемента, якая захоўвае яго ўласцівасці і складаецца з ядра і электронаў.
[Ад грэч. atomos — непадзельны.]
Тлумачальны слоўнік беларускай мовы (1977-84, правапіс да 2008 г.)
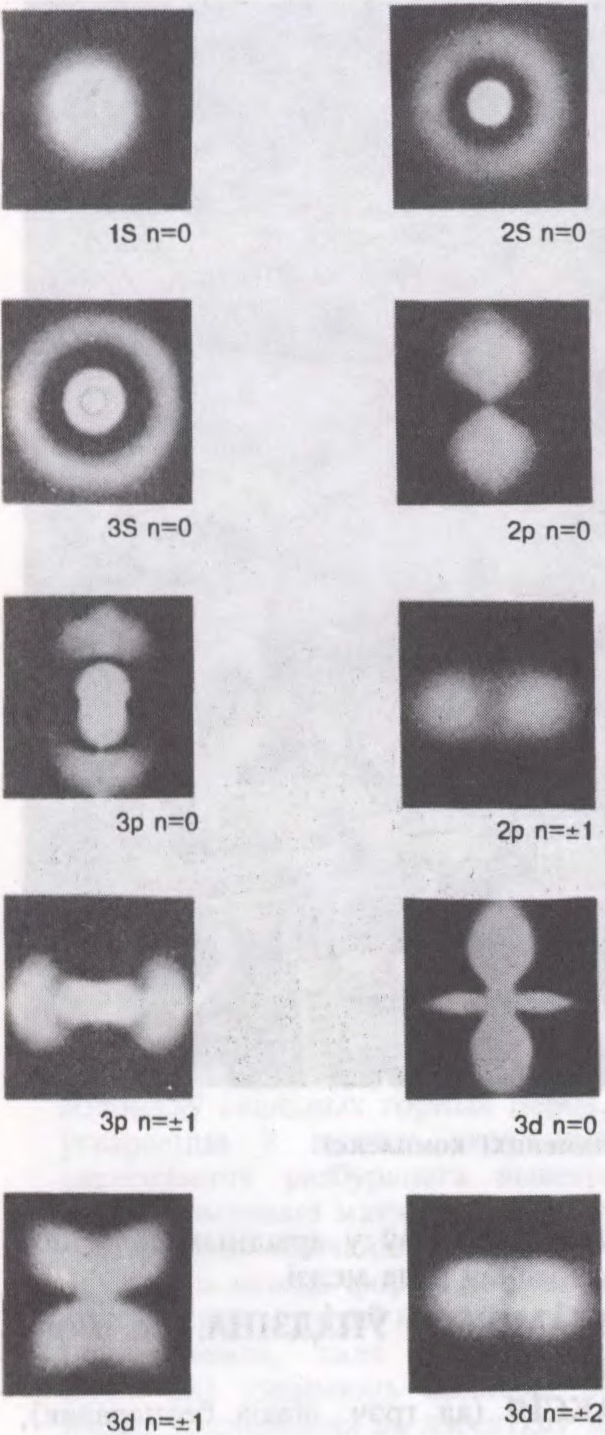
А́ТАМ (ад
часціца рэчыва, найменшая частка
Літ.:
Шпольский Э.В. Атомная физика.
Борн М. Атомная физика.
Гольдин Л.Л., Новикова Г.И. Введение в квантовую физику.
Ландау Л.Д., Лифшиц Е.М. Теоретическая физика.
Нерелятивистская теория. 4 изд.
М.А.Ельяшэвіч.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
а́там, -а,
Найдрабнейшая часцінка хімічнага элемента, якая захоўвае яго ўласцівасці і складаецца з ядра і электронаў.
||
Тлумачальны слоўнік беларускай літаратурнай мовы (І. Л. Капылоў, 2022, актуальны правапіс)
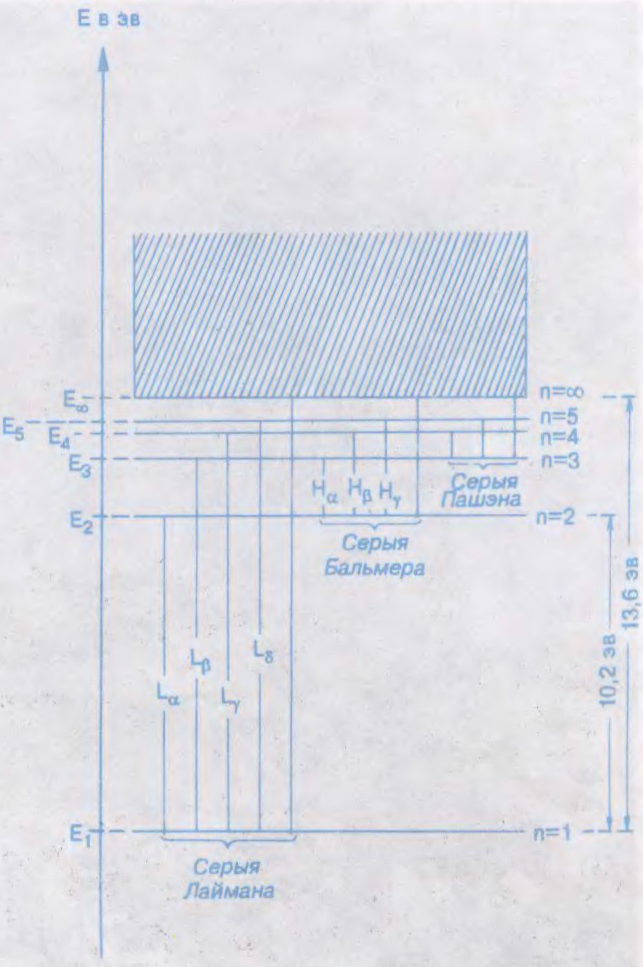
БО́РА ТЭО́РЫЯ,
першая тэорыя
Пастулаты Бора пацверджаны эксперыментальна і выконваюцца для ўсіх мікрасістэм (атамных ядраў, атамаў, малекул і
Літ.:
Ельяшевич М.А. Развитие Нильсом Бором квантовой теории атома и принципа соответствия // Успехи физ. наук. 1985. Т. 147,
М.А.Ельяшэвіч.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ВІНІ́Л,
аднавалентны астатак (радыкал) этылену CH2==CH—, які ўводзяць у малекулы
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
фи́зика фі́зіка, -кі
теорети́ческая фи́зика тэарэты́чная фі́зіка;
прикладна́я фи́зика прыкладна́я фі́зіка;
фи́зика а́тома фі́зіка
Руска-беларускі слоўнік НАН Беларусі, 10-е выданне (2012, актуальны правапіс)
КААРДЫНАЦЫ́ЙНАЯ СУ́ВЯЗЬ,
від хімічнай сувязі, якая рэалізуецца ў комплексных злучэннях. Адрозніваюць двух- і шматцэнтравую К.с. Двухцэнтравая абумоўлена перадачай электроннай пары з цалкам запоўненай арбіталі
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
трыто́н3
(ад трытый)
ядро
Слоўнік іншамоўных слоў (А. Булыка, 1999, правапіс да 2008 г.)
А́ТАМНЫ НУ́МАР,
нумар хімічнага элемента ў перыядычнай сістэме элементаў Мендзялеева. Роўны ліку пратонаў у атамным ядры. Вызначае
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)