МУАСА́Н ((Moissan) Анры) (28.9.1852, Парыж — 20.2.1907),
французскі хімік, заснавальнік хіміі цвёрдага цела.
Літ.:
Манолов К. Великие химики:
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МУАСА́Н ((Moissan) Анры) (28.9.1852, Парыж — 20.2.1907),
французскі хімік, заснавальнік хіміі цвёрдага цела.
Літ.:
Манолов К. Великие химики:
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
МУРАШЫ́НАЯ КІСЛАТА́,
найпрасцейшая аднаасноўная карбонавая
Бясколерная вадкасць з рэзкім пахам, tпл 8,4
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
НЕ́РНСТА ТЭАРЭ́МА,
адно з
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ВУГЛЯВО́ДЫ,
гліцыды, цукры, вялікая група складаных
С.А.Вусанаў.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ГІДРО́ЛІЗ (ад гідра... + ...ліз),
рэакцыя абменнага ўзаемадзеяння паміж рэчывам і вадой.
Пры гідролізе солей, утвораных слабай асновай і моцнай к-той (
Т.П.Цэдрык.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
ГО́РНЫЯ ПАРО́ДЫ,
шчыльныя або рыхлыя прыродныя мінеральныя агрэгаты больш ці менш пастаяннага мінералагічнага і
Утвараюцца ў выніку
На Беларусі ўсе класы горных парод вядомы ў складзе асадкавага чахла
У.Я.Бардон.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
КАЛО́ІДНАЯ ХІ́МІЯ,
навука, якая вывучае ўласцівасці гетэрагенных высокадысперсных сістэм і працэсы, што ў іх адбываюцца.
К.х. як
На Беларусі даследаванні па К.х. пачаліся ў
Літ.:
Воюцкий С.С. Курс коллоидной химии. 2 изд.
Щукин Е.Д., Перцов А.В., Амелина Е.А. Коллоидная химия. 2 изд.
Фридрихсберг Д.А. Курс коллоидной химии. 3 изд. СПб., 1995.
Ф.М.Капуцкі.
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
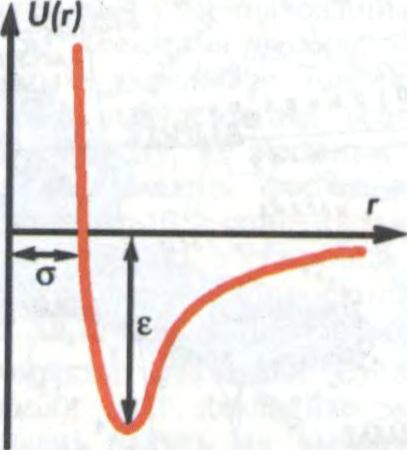
МІЖМАЛЕКУЛЯ́РНАЕ ЎЗАЕМАДЗЕ́ЯННЕ,
узаемадзеянне паміж малекуламі з насычанымі
Характар М.ў. залежыць ад адлегласці паміж малекуламі (r). Пры вялікіх r (r≫l, дзе l — лінейныя памеры малекул, што ўзаемадзейнічаюць) электронныя абалонкі малекул не перакрываюцца, паміж малекуламі пераважаюць сілы прыцягнення (далёкадзейныя сілы), якія маюць
Літ.:
Межмолекулярные взаимодействия: От двухатомных молекул до биополимеров:
Беларуская Энцыклапедыя (1996—2004, правапіс да 2008 г., часткова)
verpúffen
1.
2.
1) расстраля́ць (усе патроны)
2) растра́ціць (дарэмна) (сваю энергію, сілы)
Нямецка-беларускі слоўнік (М. Кур'янка, 2006, правапіс да 2008 г.)
nieczynny
nieczynn|y1. які не працуе (не дзейнічае);
2.
Польска-беларускі слоўнік (Я. Волкава, В. Авілава, 2004, правапіс да 2008 г.)